Антрациклины и, в особенности, доксорубицин, являются едва ли не самыми востребоӯванными цитостатиками, используемыми в хиӯмиотерапии местно-распространенного (ТЗ-4N1-3M0) рака молочной железы, несмотря на кардиотоксический эффект, впервые выявленӯный у рубомицина еще в клинической практике в конце 60-х годов [1, 2, 3, 4]. Известно, что увеӯличение кумулятивной дозы антрациклинов веӯдет к повышению кардиотоксического эффекта. В то же время, больные с местно-распространенным раком молочной железы вынуждены полуӯчать до 8-10 курсов полихимиотерапии с приӯменением антрациклинов.
В сравнении с остальной популяцией люӯдей, с выживаемостью более 5 лет после лечеӯния злокачественных опухолей с применением антрациклинов, риск смертности, связанной с сердечной патологией возрастает в 10 раз [6]. Так, при кумулятивной дозе антрациклинов менее 400 мг/м2 застойная сердечная недостаӯточность регистрируется у 3% больных, менее 550 мг/м2 - в 7% и более 700 мг/м2-в 18% слуӯчаев [5]. Причем, общая «критическая доза» доксорубицина, способная вызвать застойную сердечную недостаточность, может быть горазӯдо ниже общепринятой 550 мг/м, а именно - менее 300 мг/м.
Кардиотоксический эффект антрациклиӯнов проявляется развитием кардиомиӯопатии. Субклинические формы нарушения систолиӯческой функции левого желудочка, по данным эхокардиографии, выявляются у 14% пациентов спустя 4-6 лет после окончания химиотераӯпии антрациклинами, в 24% случаев — через 7-9 лет и у 38% — в течение 10 лет. Клиничесӯкие признаки застойной сердечной недостаточӯности появляются у 8% больных через 7-9 лет и у 15% - спустя 10 лет [6].
Выделяют 3 формы кардиотоксичности, вызванной антрациклинами. Острая форма - проявляется нарушениями ритма, клиническиӯми проявлениями перикарӯдита, миокардита или острой левожелудочковой недостаточносӯтью в период лечения или в течение месяца посӯле окончания терапии. Встречается сравнительӯно редко. Клинические проявления хроничесӯкой формы аналогичны острой форме, возникаӯют в течение года, встречаются чаще. Поздние формы антрациклиновой кардиотоксичности соответствуют проявлением острой и хроничесӯких форм с наличием или отсутствием эхокардиографических признаков левожелудочковой дисфункции; регистрируется спустя годы после окончания химиотерапии.
Так или иначе, любая из форм кардиотокӯсичности, вызываемая антрациклинами (преӯжде всего, доксорубицином), представляет сеӯрьезную клиническую проблему.
К факторам риска, повышающим вероятӯность возникновения кардиотоксического дейсӯтвия антрациклинов относят: женский пол, возӯраст более 65 лет, наличие в анамнезе заболеваӯний сердечно-сосудистой системы (гипертониӯческой болезни, атеросклероза и др.), нарушение коронарного и периферического кровообращения, превышение разовой дозы доксорубицина 50 мг/м и общей — 550 мг/м , назначение совӯместно с другими цитостатиками [7].
Изучены различные пути предупреждения кардиотоксического действия антрациклинов, включая ограничение сферы их применения в химиотерапии злокачественных опухолей, что немедленно сказалось на общей эффективности этого метода и оказалось неприемлемым. В клиӯнической практике при использовании антраӯциклинов риск кардиотоксичности далеко не всегда проявляется и осознается в период лечеӯния, оказывается несопоставимым с эффективӯностью лечения. Попытки снижения разовой и, в особенности, кумулятивной дозы антрацикӯлинов, от которой явно зависит частота кардиоӯтоксичности, приводят к снижению частоты объективного ответа на лечение. Интенсивӯность химиотерапии (дозы препаратов, получаӯемые в пересчете на одну неделю), являющаяся важнейшим фактором лечебного эффекта, приӯвела к идее снижения концентрации антрацикӯлинов в крови в единицу времени за счет проӯлонгированного введения. Действительно, разӯделение дозы, планируемой на весь 3-х недеӯльный цикл, на 3 введения, уменьшает частоту острой, но не хронической или поздней кардиоӯтоксичности. Более длительные инфузии (в теӯчение суток и более) препаратов привели к более резкому возрастанию других видов токсичносӯти и, в частности, мукозитов, что оказалось неӯприемлемым.
Современным кардиопротектором является препарат Кардиоксан. Его механизм действия связан с удалением железа из комплекса Fe-доксорубицин с помощью соединений, обладаюӯщих свойствами хелатов (связывающихся с меӯталлами и способствующими их удалению из организма), что, как было выяснено, ведет к обӯрыву цепи реакций, приводящих к образоваӯнию свободных радикалов и, соответственно, предупреждению их повреждающего действия на миокард. К сожалению, применение Кардиксана для рутинного использования ограничено его стоимостью.
Механизмы противоопухолевого действия антрациклинов заключаются, прежде всего, в подавлении синтеза ДНК, формировании ее разрывов, образовании свободных радикалов кислорода, ингибирующего влияния на ключеӯвой фермент репарации ДНК – топоизомеразу II с индукцией программы клеточной гибели -апоптоза. Из перечисленных механизмов наӯименьшее значение для цитостатиӯческого дейсӯтвия на опухоль и, наоборот, наибольшее для кардиотоксического, имеет образование свободӯных радикалов кислорода. Различия в механизӯмах противоопухолевого и кардиотоксического действия антрациклинов создают принципиӯальные предпосылки для применения патогенетических действующих протекторов кардиоӯтоксического действия этих препаратов без ущерба для противоопухолевого эффекта.
В целях снижения кардиотоксического действия антрациклинов в качестве «ловушки» свободных радикалов кислорода был применен 1,5% раствор для инфузий «Реамберин» (НТФФ «Полисан», г. Санкт-Петербург, номер регистрации № 001048/01-2002, область дейсӯтвия сертификата: территория Российской Феӯдерации). «Реамберин» представляет собой 1,5% полиионный раствор натрия - сукцината для инфузии с добавлением солей калия, наӯтрия, магния, N-метиламмония. Основной фарӯмакологический эффект препарата обусловлен способностью усиливать компенсаторную актиӯвацию аэробного гликолиза, снижать степень угнетения окислительных процессов в цикле Кребса, дыхательной цепи в цепи митохондрий клеток. С увеличением внутриклеточного фонӯда макроӯэргических соединений (АТФ и КФ) и стабилизацией клеток (кардиомиоцитов, гепатоцитов и других клеток организма). Применеӯние физиологических доз натрий-сукцината вызывает следующие эффекты: прямое дейсӯтвие на клеточный метаболизм, на транспорт свободного кислорода в ткани, нормализует аэӯробную фазу тканевого дыхания. «Реамберин» обладает антигипоксическим и антиоксидант-ным действием, оказывая положительный эфӯфект на аэробные процессы в клетке, уменьшая продукцию свободных радикалов и восстанавӯливая энергетический потенциал клеток. Преӯпарат способствует утилизации жирных кислот и глюкозы клетками, нормализует кислотно-основной баланс [8].
Превращение янтарной кислоты в организӯме связано с продукцией энергии, необходимой для жизнедеятельности. При возрастании наӯгрузки на любую систему организма поддержаӯние ее работы обеспечивается преимущественно за счет окисления янтарной кислоты. Мощӯность системы энергопродукции, используюӯщей янтарную кислоту, в сотни раз превосходит все другие системы энегообразования организӯма.
При применении физиологических доз янӯтарной кислоты выявлены 2 ведущие группы эффектов:
Влияние янтарной кислоты на трансӯпорт свободного кислорода в ткани;
Прямое действие янтарной кислоты на клеточный метаболизм.
Антиоксидантное действие «Реамберин» обусловило увеличение потребления кислорода при его применении за счет окисления добавӯленных субстратов до конечных продуктов — угӯлекислоты, воды и тепла. Иными словами, окисление янтарной кислоты является необхоӯдимым условием каталитического действия других карболовых кислот для усвоения ткаӯнью кислорода (цикл три- и дикарбоновых кисӯлот).
В проводимом нами исследовании у 200 больных местно-распространенным (ТЗ-4N1-3M0) раком молочной железы до начала химиотерапии данных о наличии сердечно-соӯсудистой патологии, исходя из жалоб, данных анамнеза, пальпации, перкуссии, аускультации, ЭКГ, ЭХоКГ, холтеровского мониторирования не было.
После проведения 4 курсов полихимиотеӯрапии (ПХТ) по схеме CAF (циклофосфан 100 мг/м2 1-14 день в/м, адриамицин 30 мг/м2 в 1 и 8 день в/в, фторурацил 500 мг/м в 1 и 8 день в/в) у больных местно-распространенӯным раком молочной железы без «Реамберина» (100 больных) уже после первого курса ПХТ 54 пациента (54,0%) отмечали учащенное сердӯцебиение, эпизоды подъема АД, боли за грудиӯной и др. По данным ЭКГ после 3-го курса ПХТ по схеме CAF у 26 пациентов (26,0%) были выӯявлены признаки перегрузки левого желудочӯка. По данным ЭХоКГ после 4 курса у 36 пациентов (36,0%) определялось снижение фракции выброса левого желудочка (Рис. 1).
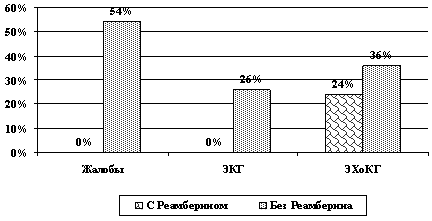
Рис. 1. Сравнительная характеристика
кардиальных изменений
при проведении химиотерапии с использованием препарата Реамберин и без него
По данным холтеровского мониторирования у 82 пациентов (82,0%) после 4 курса ПХТ была выявлена суправентрикулярная экстрасистолия, у 64 пациентов (64,0%) - метаболиӯческие изменения в конечной части желудочкоӯвого комплекса в виде снижения вольтажа и инӯверсии зубца Т.
Пациенты, получающие химиотерапию по схеме CAF с «Реамберином» (100 больных), не имели кардиальных жалоб. По ЭКГ признаков перегрузки левого желудочка не было. На ЭХоКГ зарегистрировано снижение фракции выӯброса левого желудочка у 24 пациентов (24,0%). Суправентрикулярная экстрасистолия по данным холтеровского мониторирования отмечена у 42человек (42,0%), метаболиӯческие изменения в конечной части желудочкоӯвого комплекса в виде снижения вольтажа и инӯверсии зубца Т - у 23 больных (23,0) (Рис. 2).
Следует отметить, что кумулятивные дозы доксорубицина за время проведения четырех курсов по схеме CAF были довольно высокими – в среднем 500 мг/м2. Среди 100 больных, полуӯчивших полную дозу доксоруӯбицина, не было ни одного случая застойной сердечной недостаӯточности или снижения фракции выброса левоӯго желудочка (LVEF) менее 45% от исходного. Также не было отмечено влияния препарата «Реамберин» на уровень противоопухолевого эффекта.
Методика применения «Реамберина», обеспечивающая протекторный эффект против кардиотоксичности антрациклинов. Рекоменӯдуется использовать «Реамберин» внутривенно капельно медленно со скоростью 2 мл/минуту по 400 мл в течение 5-ти дней во время проведеӯния полихимиотерапии местно-распространен-ного рака молочной железы.
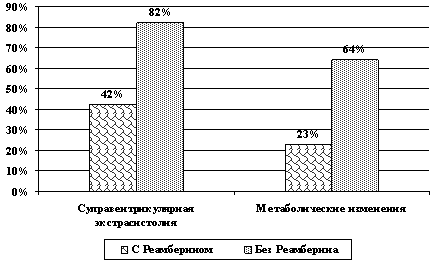
Рис. 2. Сравнительная характеристика
кардиальных изменений
при проведении химиотерапии с использованием препарата
Реамберин и без него
Среди побочных эффектов у 1 пациентки отмечена аллергическая реакция в виде залоӯженности носа, исчезнувшая самостоятельно при снижении скорости введения препарата.
Все представленное выше позволяет заклюӯчить, что «Реамберин» действительно является безопасным протектором кардиотоксичности антрациклинов. Применение «Реамберина», не сопровождающееся ослаблением противоопуӯхолевого эффекта антрациклинов, позволяет проводить лечение без риска инвалидизирующих кардиальных последствий больных местнораспространенным раком молочной железы. Вероятно, использование «Реамберина» позвоӯлит повысить интенсивность химиотерапии антрациклинами в моно режиме или в комбинаӯции с другими цитостатиками у взрослых и деӯтей со злокачественными опухолями разӯличных локализаций и тем повысить ее эффекӯтивность. Совокупность сведений о «Реамбе-рине» показывает, что имеются все основания не только для широкого применения препарата в онкологической практике, но и для дальнейӯшего клинического углубленного изучения поӯлезных свойств препарата в различных направӯлениях.
Список литературы
1. Гершанович МЛ. Осложнения при химио- и гормонотерапии злокачественных опухолей.— М.: Медицина, 2004.- 15 с.
2. Epirubicin Hydrochloride: Integrated Summary of efficacy. Data on file, Pharmacia, November 19, 1998.
3. Smith P., Soues S. Multilevel therapeutic targeting by topoisomerase inhibitors. Br J Cancer 1994; 23: S 47.
4. Cersosimo R.G. Hong W.K. Epirubicin: a review of farmacology, clinical activity and adverse effect of an adriamicin analogue. J Clin Oncol 1986; 4: 425-39.
5. Launcbbury A.P., Habboubi N. Epirubicin and doxorubicin: a comparison of their characneristics, therapeutic activity and toxicity. Cancer Treat Rev 1993;19:197.
6. Fisher В., Redmond C. et al. Doxorubicin - conӯtaining regimens for the stage 2 breast cancer: J Clin Oncology 1989; 7: 572.
7. Стенина М.Б. Эпирубицин (Фармарубицин) в адъювантной терапии рака молочной железы. // Совӯременная онкология.- 2004.- № 1.-Т6.- С. 20.
8. Романцов М.Г. Реамберин - инфузионный раствор для интенсивной терапии в педиатрической практике. // Сборник статей НТФФ «Полисан» -2002,-СПб.-С. 6-9.
Summary
In article cited the data on reduction cardiotoxice effect of polychemotherapy of the local-widespread canӯcer mammary gland with the Reamberinum. Reamberinum really is a safe protector cardiotoxice effect anthracyclines. Application Reamberinum, is not accompanied by easing of antineoplastic effect anthracydines, allows to carry out treatment without risk of development cardial complications at patients with the local-widespread cancer mammary gland. Use Reamberinum allows to increase intensity of chemotherapy with anthracyclines in monotherapy or in a combination with others cytostatics at adults and children with malignant tumours of various localizations promoting increase its efficiency.