Частота возникновения и тяжесть клинических проявлений синдрома
полиорганной недостаточности, возникающего как
функционально-морфологический результат многокомпонентных каскадов
постгипоксических расстройств тканевого метаболизма при любом
критическом состоянии, напрямую зависит от неспецифической
резистентности организма, в частности, и прежде всего от
резистентности к гипоксии.
Уровень повреждения и саногенеза окислительно-восстановительных
систем тканевого дыхания различных органов и систем в условиях
критического состояния можно корригировать различными методами
фармакологической защиты, применяя антигипоксанты и антиоксиданты
различных групп. Высокая чувствительность к
химико-фармакологической агрессии при лечении критических состояний
делает применение препаратов разнонаправленного действия опасными
для пациентов и ведет к полипрагмазии.
Использование препарата Реамберин, обладающего многокомпонентным
антигипоксическим, антиоксидантным, дезинтоксикационным, гепато-,
нефро- и кардиопротекторным действием становится особенно
целесообразным в условиях высокой вероятности полиорганных тканевых
постгипоксических расстройств.
Цель и задачи исследования
Целью клинического изучения препарата Реамберин при критических
состояниях различного генеза, прежде всего при шоках, гипоксии и
интоксикациях, являлось выявление его влияния как антигипоксанта,
антиоксиданта и гепатопротектора на возникновение, развитие и
прогрессирование различных клинических проявлений синдрома
полиорганной недостаточности, развивающегося у большей части
больных в результате перенесенного терминального состояния.
Основной задачей было выявление клинико-параклинических критериев
целесообразнсть применения препарата и последующая разработка
оптимальных схем его использования у больных, перенесших
критические состояния.
Группы больных
Исследование проведено у 22 больных, разделенных на три группы:
1-я – больные с постгипоксическими состояниями различной
этиологии; 2-я – больные с распространенными перитонитами; 3-я –
больные с тяжелыми сочетанными травмами, которым в комплекс терапии
был включен реамберин. Контрольная группа – 30 человек, которым
проводилась общепринятая интенсивная фармакотерапия.
Метод лечения
В комплексе терапии критических состояний 1,5% раствор
Реамберина использовали в суточной дозе 400 мл раствора со
скоростью 20-30 капель в минуту в течение первых двух-трех суток
от момента развития критического состояния.
В ходе клинического изучения препарата реамберин было выявлено
несомненное положительное его влияние на течение заболеваний у
больных, перенесших критическое состояние.
Данное положительное влияние было выявлено у 80% больных. Оно
проявлялось, прежде всего, в активации состояния сознания у всех
больных с явлениями постгипоксической энцефалопатии, у 50% больных
с сочетанной травмой и перитонитом.
При этом необходимо отметить, что динамика состояния сознания
выявлялась даже при исходно глубоком его угнетении (до 5-6 баллов
по шкале комы Глазго).
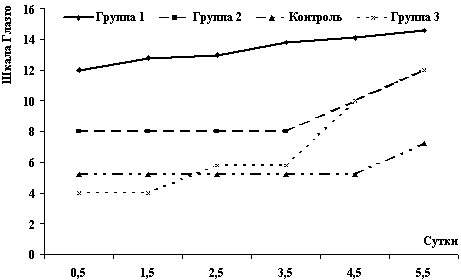
Рис. 10. Динамика состояния сознания на фоне лечения
реамберином
Подобные клинические наблюдения (2 случая) довольно быстрой (на
2-3 сутки) динамики состояния сознания у больных с
постгипоксической энцефалопатией с фоновым уровнем расстройств
сознания до 5-6 баллов по шкале комы Глазго являются чрезвычайно
важными для оценки результатов данного исследования. Они
убедительно говорят о целесообразности и необходимости применения
Реамберина в качестве антигипоксанта и антиоксиданта в ранние
сроки постгипоксического поражения мозга у больных с терминальными
состояниями.
Отмечена была также активация функциональной активности
головного мозга по данным мониторинга электроэнцефалограммы.
Отмечено нарастание быстроволновой части спектра ЭЭГ по сравнению с
медленноволновой, что, несомненно, является благоприятным
электрофизиологическим признаком. Однако, отмечается и увеличение
суммарной мощности спектра ЭЭГ после применения Реамберина
составляет до 24-28% от фонового.
Увеличение суммарной мощности спектра ЭЭГ наряду с активацией
состояния сознания говорит о значимой активации
окислительно-восстановительных процессов в тканях мозга под
действием Реамберина.
Максимальный клинический и электрофизиологический эффект
Реамберина проявлялся у больных с фоново низким уровнем суммарной
мощности спектра.
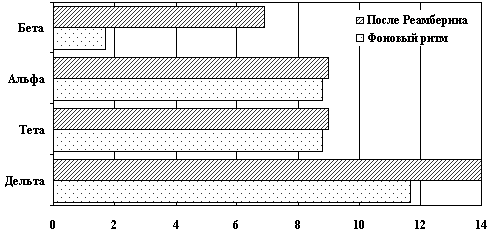
Рис. 11. Корковая активность головного мозга (по данным ЭЭГ)
до и после лечения
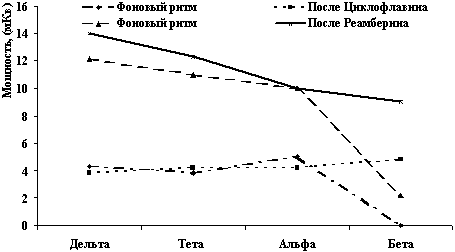
Рис. 12. Корковая активность головного мозга (по данным
ЭЭГ) до и после применения препаратов, содержащих янтарную кислоту
Другие параклинические параметры, прежде всего, динамика
кислотно-щелочного состояния крови больных на фоне применения
реамберина также были положительными (рисунок 13).
Аллергических реакций на фоне применения препарата ни в одном
случае отмечено не было. Препарат всегда хорошо переносился и не
имел побочных эффектов.
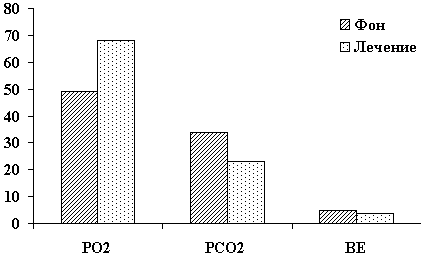
Рис. 13. Динамика КОС на фоне лечения Реамберином
Таким образом, включение реамберина в комплексную терапию
постгипоксических расстройств у больных, перенесших критическое
состояние, несомненно способствует повышению резистентности к
гипоксии и снижению выраженности клинических проявлений синдрома
полиорганной недостаточности, в частности, энцефалопатии.
Основной фармакологический эффект препарата обусловлен
способностью усиливать компенсаторную активность аэробного
гликолиза, снижать степень угнетения окислительных процессов в
цикле Кребса в условиях гипоксии с увеличением содержания АТФ и
креатинфосфата, Реамберин активируетантиоксидантную систему
ферментов и тормозит процессы перекисного окисления липидов в
ишемизированных органах, оказывая мембраностабилизирующее
действие.
СИНДРОМ ПОЛИОРГАННОЙ НЕДОСТАТОЧНОСТИ
У БОЛЬНЫХ ПЕРИТОНИТОМ
Перитонит - воспаление брюшины, сопровождающееся нарушениями
функций жизненно важных органов и систем. При разлитом перитоните
наблюдаются выраженные нарушения гомеостаза с развитием
полиорганной недостаточности. (ПОН).
Несмотря на современные достижения медицины: индивидуальный
выбор метода оперативного вмешательства, применение комплексной
антибактериальной терапии, применение эфферентных методов лечения и
т.д., летальность при разлитом перитоните колеблется от 22 до 45%.
При запущенном Перитоните с уже выраженными явлениями эндотоксикоза
летальность достигает более 80 процентов.
ПОН — это поражение всех органов и тканей агрессивными
медиаторами критического состояния с временным преобладанием той
или иной органной недостаточности — легочной, сердечной, почечной и
т.д.
Выделяют несколько механизмов развития полиорганной
недостаточности:
- медиаторных, при котором рассматривают ПОН как аутоиммунное
поражение;
- микроциркуляторный и связанный с ним реперфузионный
механизм;
- инфекционно-септический механизм, с которым связывают гипотезу
"кишечник как не дренированный абсцесс".
В последние годы неоспоримым считается, что эндотоксикоз (ЭТ) и
энцефалопатия являются наиболее яркими и информативными симптомами
в проявлении ПОН. Снижение уровня эндогенной интоксикации и
нормализация высшей нервной деятельности носят прогностический
характер.
Однако оценка степени эндотоксикоза до сих пор представляет
определенные трудности, несмотря на множество предложенных методов
(Шимкевич Л.Л., (1982); Николайчик В.В., (1985); Кузнецов В.А.,
Анисимов А.Ю., (1995)).
Наиболее серьезные нарушения ЭТ наблюдаются в показателях
белкового обмена, что связано с угнетением синтеза белков и
усилением их катаболизм. Важным звеном является альбумин-белок,
выполняющий пластические и транспортные функции. Снижение
содержания этого белка служит важнейшим прогностическим признаком
интоксикации и выживаемости (Чегер С.Н., (1975)). При тяжелом ЭТ в
организме создаются условия для образования форм альбумина с
измененными физико-химическими характеристиками, "перегруженного"
лигандами, что препятствует обмену между тканями и сосудистым
руслом и транспортом токсинов к органам
детоксикации-биотрансформации. Поэтому особый интерес вызывают
методы, позволяющие судить не только о количестве, но и о структуре
и функциональной активности альбумина.
Был создан и внедрен в клиническую практику флуориметр АКЛ-01 и
наборы реактивов "ЗОНД-Альбумин", позволяющие контролировать общую
концентрацию альбумина (ОКА) в крови, эффективную концентрацию
альбумина (ЭКА), его связывающую способность (РСА – резерв
связывания альбумина), и рассчитывать "индекс токсичности"
(Т=ОКА/ЭКА - 1).
Использование этих показателей наряду с общеизвестными
клиническими тестами (клинический анализ крови, Билирубин, уровень
трансаминаз и фосфатаз в крови, уровень молекул средней массы,
уровень электролитов в плазме крови, протеинограмма) позволяют
оценить уровень ЭТ, а также по их изменениям оценить эффективность
лечения.
Другим важным критерием эндотоксемии является степень
выраженности энцефалопатии. Критерием оценки энцефалопатии всегда
являлась оценка уровня сознания. В последние годы появились
приборы, позволяющие объективно оценивать функциональную активность
головного мозга в динамике. Энцефалографический монитор фирмы
Drager (Германия) позволяет проводить длительное динамическое
наблюдение всех стандартных параметров энцефалограммы по двум
полушариям. При этом на экран монитора выводится нативная
энцефалограмма по двум отведениям. Одновременно производится
компрессированный спектральный анализ энцефалограммы с выведением
на экран монитора трендов спектра ЭЭГ по обоим полушариям в двух
стандартных режимах (частоты и амплитуды составляющих спектра ЭЭГ).
Динамика ЭЭГ при визуальной оценке нативной ЭЭГ и особенно при
количественном подсчете спектральных составляющих по амплитуде и
частотам является одним из наиболее аргументированных и достоверных
методов оценки функциональной активности головного мозга.
Энцефалограмма, как конечная результирующая электрогенеза мозга
отражает как некоторые очаговые изменения, так и выраженность
поражения мозга в целом. Как показано многочисленными
исследованиями (Safar, (1976); Revers, (1990); Sidi, (1990); Dick,
(1992)) параметры ЭЭГ и их динамика коррелирует с уровнем
мозгового кровотока и определяется как состоянием кровотока, так и
газовым составом крови, притекающей к мозгу.
Таким образом, анализ ЭЭГ может служить объективным критерием
состояния кислородного баланса и уровнем метаболитов (эндотоксинов)
в мозге при различных патологических воздействиях.
ЦЕЛЬ РАБОТЫ заключалась в изучении клинической
эффективности препарата Реамберин 1,5% для инфузий в качестве
дезинтоксирующего средства у больных с перитонитом при развитии у
них синдрома полиорганной недостаточности.
ЗАДАЧИ ИССЛЕДОВАНИЯ:
- Определить влияние препарата Реамберин 1,5% для инфузий на
динамику клинико-лабораторных показателей у больных перитонитом при
развитии синдрома ПОН;
- Определить влияние препарата Реамберин 1,5% для инфузий на
уровень эндотоксикоза у больных перитонитом при развитии синдрома
ПОН;
- Определить влияние препарата Реамберин 1,5% для инфузий на
динамику ЭЭГ у больных перитонитом при развитии синдрома ПОН.
КРИТЕРИИ ВКЛЮЧЕНИЯ В ИССЛЕДОВАНИЕ:
Пациенты с перитонитом при развитии у них синдрома ПОН,
удовлетворяющие следующим требованиям: возраст от 20 до 70 лет.
1) наличие перитонита и синдрома ПОН;
2) оперированные по поводу разлитого перитонита по однотипным
методикам:
3) имеющие органные нарушения ЦНС в начальных сроках
заболевания.
Письменное информированное согласие больного или
родственников на исследование.
ГРАФИК КЛИНИЧЕСКОГО ОБСЛЕДОВАНИЯ БОЛЬНЫХ:
Комплексное клинико-лабораторное и инструментальное обследование
проводилось в 2-х группах:
- контрольной – без применения препарата;
- опытной – с применением препарата.
В обеих группах больным проводилась комплексная, принятая в
отделении реанимации ГКБ № 15 корригирующая терапия, направленная
на лечение перитонита и проявлений синдрома ПОН.
Обследование больных осуществляли в следующих точках:
- До начала лечения, в момент поступления больного в отделение
реанимации;
- На следующий день после введения препарата;
- На 3-й, 5-й и 8-й дни от начала лечения препаратом Реамберин
1,5% инфузий.
ОЦЕНКА ЭФФЕКТИВНОСТИ
ПРЕПАРАТА РЕАМБЕРИН 1,5% ДЛЯ ИНФУЗИЙ
Эффективность лечения препаратом определялась по следующим
показателям:
- клиническое состояние больного до и после лечения;
- динамика стандартных клинико-лабораторных показателей в процессе
лечения;
- динамика уровня ЭТ в процессе лечения;
- динамика спектра ЭЭГ в процессе лечения;
- сравнение полученных данных с аналогичными показателями у
больных ко трольной группы.
Схема введения препарата Реамберин 1,5% для инфузий:
Препарат Реамберин вводился внутривенно капельно в количестве
400 мл. и фузионного раствора в сутки согласно инструкции по
клиническому изучению в течение 7 дней, начиная со 2-го дня от
поступления больного в отделение реанимации.
Клинические исследования проводились по методу мультицентрового
испытания по единой программе при эндогенной интоксикации,
обусловленной ПОН. Исследование открытое, контролируемое,
рандомизированное.
Для проведения исследования были сформированы следующие группы
больных:
- больные разлитым перитонитом с клиническим проявлениями и
лабораторными показателями синдрома полиорганной недостаточности
25 человек - 1-я группа больных, основная;
- больные разлитым перитонитом с клиническими проявлениями и
лабораторными показателями синдрома полиорганной недостаточности
10 человек – 2-я группа больных, контрольная.
Среди пациентов мужчин было 19, женщин — 14.
Средний возраст больных составлял 53±3,1 года.
Клиническая оценка была основана на осмотре врача при
поступлении больного в отделение реанимации, оценке уровня
сознания по шкале Глазго, оценке общего состояния пациента по шкале
SAPS. Биохимические исследования включали в себя определение
уровня калия и натрия в плазме, уровней билирубина, мочевины,
креатинина, общего белка и альбумина, щелочной фосфатазы,
трансаминаз, гаммаглютаматтрансфераз, сахара крови на
биохимическом анализаторе Express 550, уровня МСМ по способу
Малаховой М.Я. (Малахова М.Я, (1995)), калия и натрия в эритроцитах
методом плазменной фотометрии; осмолярность плазмы и мочи на
осмометре производства ГДР; КОС на анализаторе Corning, уровни ОКА,
ЭКА, РСА И Т определяли на отечественном приборе "ЗОНД" по
методике, предложенной НИИ ФХМ РАМН (Е.Е. Добрецов); ЭЭГ-контроль
осуществляли прикроватным электроэнцефалографом фирмы Drager
(Германия).
Клинические исследования показали, что на фоне применения
Реамберина отмечено снижение уровня тяжести состояния пациентов по
шкале SAPS (таблица 49).
Таблица 49. Тяжесть состояния пациентов по шкале SAPS
|
Группы
больных
|
До
введе-
ния
|
1
сутки
|
3
сутки
|
5
сутки
|
8
сутки
|
|
Основная Контрольная
|
13.8
14.2
|
10.4
12.2
|
9.3
11.2
|
6.8
9.0
|
5.5
6.5
|
Как видно из приведенной таблицы тяжесть состояния больных
оценена как тяжелая. Согласно правилам пользования системой SAPS к
тяжелым относятся пациенты, Набравшие более 12 баллов. В процессе
лечения больные, получавшие Реамберин были склонны к более быстрому
восстановлению, что выражалось в уменьшении числа баллов по шкале
SAPS.
Анализ основных лабораторных тестов показал, что у больных обеих
групп, на фоне введения препарата Реамберин отмечается четкая
тенденция к более быстрому купированию метаболического ацидоза,
нормализации клеточного и плазменного калия, уменьшению, уровней
креатинина, билирубина, щелочной фосфатазы и ACT, МСМ уже на
следующий день после введения препарата.
Анализ уровня токсемии по "альбуминовому тесту" выявил
достоверные различия в основной и контрольной группах. В таблице 50 представлены изменения "альбуминовых тестов" на фоне введения Реамберина у больных разлитым перитонитом.
Из приведенных в таблице данных видно, что у всех больных в
момент поступления в отделение реанимации имел место высокий
уровень эндотоксемии, введение препарата Реамберин позволяет
быстрее, чем в контрольной группе снизить уровень
эндотоксикоза.
ЭНЦЕФАЛОГРАФИЧЕСКИЙ МОНИТОРИНГ
У БОЛЬНЫХ ПРИ ПРИМЕНЕНИИ РЕАМБЕРИНА
У 15% больных на фоне применения реамберина (непосредственно в
ходе внутривенного капельного введения препарата и после окончания
введения препарарата) было отмечено нарастание амплитуды
электроэнцефалограммы. Всем больным указанной группы на фоне
применения Реамберина проводился длительный энцефалографический
мониторинг.
Исследования проведены с помощью энцефалографического монитора
pEEG фирмы Dreger (Германия) со специально разработанным фирменным
программным обеспечением. Энцефалографический монитор позволяет
проводить длительное динамическое наблюдение всех стандартных
параметров энцефалограммы двум отведениям, т.е. запись
энцефалограммы по двум полушариям. При этом на экран монитора
выводится нативная Энцефалограмма по двум отведениям. Одновременно
производится компрессированный спектральный анализ энцефалограммы
с выведением на экран монитора трендов спектра ЭЭГ по обоим
полушариям в двух стандартных режимах (частоты и амплитуды
составляющих спектра ЭЭГ).
Специально разработанное фирменное программное обеспечение
позволяет длительно хранить и проводить анализ спектров ЭЭГ,
полученных в режиме реального времени. Динамика
электроэнцефалограммы, при визуальной оценке нативной ЭЭГ и
особенно при количественном подсчете спектральных составляющих по
амплитуде и частотам, является одним из наиболее аргументированных
и достоверных методов оценки функциональной активности головного
мозга. Энцефалограмма, как конечная результирующая электрогенеза
мозга, отражает как некоторые очаговые изменения, так и
выраженность поражения мозга в целом при различных патологических
влияниях на него.
Как показано многочисленным исследователями (Safar, 1976; Reves,
1990; Sidi, 1990; White, 1989; Scott, 1985; Dick, 1992) параметры
ЭЭГ и их динамика коррелируют с уровнем мозгового кровотока и
определяются как состоянием кровотока, так и газовым составом
притекающей к мозгу крови.
Таким образом, анализ ЭЭГ может служить объективным критерием
состояния кислородного баланса и уровня метаболитов в мозге при
различных патологических воздействиях.
Всем больным энцефалографический церебральный мониторинг
проводили в динамике наблюдения в следующие сроки:
- При поступлении в отделение реанимации;
- На первые сутки, на 3-и и 7-е сутки применения препарата.
У части больных при длительном пребывании в отделении реанимации
исследования проводились на 10-е, 15-е, 20-е, 42-е и даже 45-е
сутки от момента поступления в отделение.
ОСОБЕННОСТИ СПЕКТРА ЭЭГ У БОЛЬНЫХ
С ТОКСИЧЕСКИМИ ЭНЦЕФАЛОПАТИЯМИ
НА ФОНЕ ПЕРИТОНИТА
Характерными особенностями спектра ЭЭГ и нативной
электроэнцефалограммы больных с токсическими энцефалопатиями при
фоновом исследовании было снижение амплитуды спектра (до 50-60%
мощности) от стандартных параметров амплитуды здоровых исследуемых.
Характерным было также значительное нарастание частот в медленно
волновом диапазоне с преимущественной выраженностью дельта волн,
которые составляли от 50 до 60% общей мощности спектра (в
стандартных условиях у здоровых лиц выраженность дельта активности
составляет не более 15% суммарной мощности спектра). На фоне
депрессии суммарной мощности спектра со сдвигом частот в медленно
волновую его часть у больных с расстройствами сознания до комы 1
(3 больных) выявлены участки более грубой депрессии нативной ЭЭГ и
ее спектра с последующим появлением нарастающих по амплитуде
медленных волн. Частоты альфа диапазона были представлены в
среднем в объеме до 17% мощности, частоты бета диапазона – до 5%
мощности.
Особенности состояния спектра ЭЭГ с постепенной депрессией его
по амплитуде и увеличением представленности медленноволновой части
спектра практически не зависели от генеза поражения мозга,
поскольку конечным пусковым механизмом повреждения всегда была
гипоксия с фоновой глубиной расстройств сознания. Наиболее грубые
нарушения амплитуды и частоты имели место у больных с
расстройствами сознания до комы 1-2, у больных с фоновым уровнем
сознания до глубокого сопора, выраженность депрессии амплитуды была
меньшей, хотя медленно волновой сдвиг прослеживался практически во
всех случаях.
В ходе клинического исследования выявлены следующие особенности
состояния электроэнцефалографической активности по данным нативной
ЭЭГ и при мониторинге ее спектра:
- до 20% суммарной мощности от фоновой за счет преимущественной
активации частот дельта- и тетта-диапазона;
- у 5% больных отмечено нарастание суммарной мощности спектра ЭЭГ
на 20% за счет активации частот альфа-диапазона.
У больных данной группы нарастание мощности спектра ЭЭГ
сопровождалось активацией состояния сознания до более высокого
уровня (практически во всех случаях от глубокого сопора до сопора
или сонливости) на фоне применения Реамберина или через 2-3 часа
после окончания инфузии.
У больных с фоновым уровнем сознания кома 1 (6%) и наиболее
грубой степенью депрессии энергетического метаболизма по данным
спектрограмм ЭЭГ - (снижение вольтажа ниже 60% от стандартного,
наличие только медленно волновой части спектра, наличие участков
биоэлектрического молчания) динамики изменений на фоне применения
Реамберина не было, активации состояния сознания не
происходило.
Положительная динамика у 8% больных по данным ЭЭГ и уровню
состояния сознания была отмечена в отсроченный период – через 5-10
суток после окончания первого курса применения препарата. У
остальных больных четкой коррелятивной устойчивой связи динамики
негативной ЭЭГ и спектра ЭЭГ с применением Peaмберина отмечено не
было.
Отрицательной динамики на уровень расстройств сознания препарат
не оказывал.
Активация состояния сознания на фоне применения Реамберина у
больных с токсической энцефалопатией имела место в 20% случаев
(учитывая фоновую глубину расстройств сознания у больных данной
группы, это может считаться хорошим показателем).
Положительная динамика по данным спектрограмм при
проведении мониторинга ЭЭГ у больных с
тяжелыми энцефалопатиями, активация состояния у части
больных, увеличение сроков жизни у больных с тяжелейшими
поражениями головного мозга, снижение летальности у
больных указанных групп позволяют рекомендовать
использование препарата Реамберин в клинической реанимационной и
нейрореанимационной практике в качестве инфузионного
нейрометаболического корректора.)
Таким образом, препарат Реамберин 1,5% для инфузий может
быть использован в терапии больных разлитым
перитонитом при развитии у больных данной группы
синдрома полиорганной недостаточности. Применение данного
препарата может быть использована как для
предоперационной подготовки больных с литым перитонитом, так н
интенсивной терапии в послеоперационный период.
Препарат может быть использован в качестве корректора
характерных для больных перитонитом и при развитии синдрома ПОН,
расстройств энергометаболизма, способствуя уменьшению выраженности
эндотоксикоза как по клинико-лабораторным, так и по
энцефалографическим параметрам.
Применение препарата позволяет увеличить период жизни
пациентов и снизить уровень летальности больных перитонитом даже
при развитии синдрома полиорганной недостаточности.
Применение препарата не вызывает аллергических реакций и
побочных эффектов, препарат может быть использован как комплексный
энергометаболит и корректор инфузионных расстройств у больных
разлитым перитонитом.
СОСУДИСТЫЕ ПОРАЖЕНИЯ МОЗГА
ПРИ СИНДРОМЕ ПОЛИОРГАННОЙ НЕДОСТАТОЧНОСТИ
Лечение больных с сосудистыми поражениями головного мозга,
прежде всего с нарушениями мозгового кровообращения, особенно в
остром периоде заболевания, в частности, выбор адекватных
фармакологических препаратов представляет собой сложную задачу.
Прежде всего, имеет значение тяжесть состояния больного,
определяемая многообразными расстройствами функций в результате
церебрального поражения, а также развивающимися в результате
поражения мозга соматическими осложнениями. Определенную роль при
этом играет разнонаправленный характер изменения функционального
состояния как мозга, так и его сосудистых бассейнов в результате
тяжелых, прежде всего, метаболических расстройств.
На одно из первых мест при как ишемическом, так и при
геморрагическом инсульте выступает не сопряженность сдвигов
гемодинамики и метаболизма, провоцирующая прогрессирование
вторичных церебральных ишемий и пост ишемических отеков головного
мозга. Ишемические и геморрагические инсульты даже при самых
современных, в том числе и хирургических, методах лечения остаются
заболеваниями с одной из самых высоких летальностей (до 45-60%)
именно из-за развития вторичных церебральных метаболически
обусловленных ишемий. Эти церебральные расстройства достаточно
часто приводят к утрате центральной нервной системой своих
регуляторно-трофических функций и быстрому прогрессированию
вторичных соматических осложнений, которые следует рассматривать
как церебрально обусловленный синдром полиорганной
недостаточности. Причем, вследствие утраты регуляторно-трофических
влияний ЦНС данный синдром у больных с церебральными заболеваниями
развивается гораздо быстрее, чем у больных с эндотоксикозами другой
этиологии.
Клинические исследования проводились по методу мультицентрового
испытания по единой программе при сосудистых поражениях мозга и
эндогенной интоксикации, обусловленной полиорганной
недостаточностью.
Исследование открытое, контролируемое, рандомизорованное.
Для проведения исследования были сформированы следующие
группы:
Больные разлитым перитонитом с сосудистыми заболеваниями
головного мозга, осложнившимися развитием ПОН (по клиническим и
лабораторным показателям) 23 человека – основная группа;
Больные с сосудистыми поражениями головного мозга с клиническими
проявлениями и лабораторными показателями синдрома полиорганной
недостаточности 15 человек — контрольная группа.
Среди пациентов мужчин было 18, женщин – 20.
Средний возраст больных составлял 52±3,1 года.
В таблице 51 представлены основные причины сосудистых
заболеваний головного мозга.
Таблица 51. Причины органных нарушений ЦНС
|
Причина нарушений
|
Контрольная группа
|
%
|
Основная группа
|
%
|
|
ОНМК по ишеми-
ческому типу
|
8
|
53,3
|
12
|
52,1
|
|
ОНМК по гемор-
рагическому типу
|
7
|
46,6
|
11
|
47,9
|
|
Всего
|
15
|
100
|
23
|
100
|
Клиническая оценка основывалась на осмотре больного при его
поступлении в отделение реанимации, оценке уровня сознания по шкале
Глазго, оценке общего состояния пациента по шкале SAPS.
Биохимические исследования включали определение уровня калия и
натрия в плазме, уровней билирубина, мочевины, креатинина, общего
белка и альбумина, щелочной фосфатази, трансаминаз,
гаммаглютаматтрансфераз, сахара крови на биохимическом анализаторе
Express 550, уровня МСМ по способу М.Я. Малаховой (Малахова М.Л.,
(1995)), калия и натрия в эритроцитах – методом пламенной
фотометрии; осмолярность плазмы и мочи – на осмометре производства
ГДР; КОС – на анализаторе Corning, уровни ОКА, ЭКА, РСА и Т
определяли на отечественном приборе "ЗОН-Д" по методике,
предложенной НИИ ФХМ РАМН (Т.Е. Добрецов); ЭЭГ-контроль
осуществляли прикроватным электроэнцефалографом фирмы Drager
(Германія).
РЕЗУЛЬТАТЫ ИССЛЕДОВАНИЙ
Клинические исследования показали, что на фоне применения
Реамберина отмечено снижение уровня тяжести состояния пациентов по
шкале SAPS (таблица 52).
У всех наблюдаемых больных состояние расценено как тяжелое.
Согласно правилам пользования системой SAPS к тяжелым относятся
пациенты, набравшие более 12 баллов. В процессе лечения больные,
получавшие Реамберин, были склонные к более быстрому
восстановлению, что выражалось в уменьшении числа баллов по шкале
SAPS.
Анализ основных лабораторный тестов показал, что у больных обеих
групп на фоне введения препарата, Реамберин отмечается четкая
тенденция к более быстрому купированию метаболического ацидоза,
нормализации клеточного и плазменного калия, уменьшению уровней
креатинина, билирубина, щелочной фосфатазы уже на следующий день
после введения препарата.
Отсутствие четкой статистической корреляции может быть объяснено
не очень большим количеством больных и большим разбросом данных
биохимических обследований у больных с тяжелыми формами сосудистых
поражений головного мозга на фоне прогрессирования ПОН.
Анализ уровня токсемии по "альбуминовому тесту" выявил
достоверные различия в основной и контрольной группах. В таблице 53 представлены изменения "альбуминовых тестов" на фоне введения
Реамберина у больных с сосудистыми поражениями головного мозга.
Как видно из данной таблицы, у больных отмечается нарастание
явлений эндотоксикоза в ходе развития заболевания, что согласуется
с клиническими данными. У больных с органическими поражениям ЦНС
острым периодом считается период до 3-х недель от начала
заболевания, когда возможно прогрессирование симптоматики. Вместе
с тем из таблицы видно, что у больных получавших Реамберин,
отмечено более медленное нарастание эндотоксикоза.
Анализ летальности показал, что у больных с заболеваниями ЦНС
летальность в среднем составляет 67,3% в контрольной группе и 46,5%
в основной.
Значимое снижение летальности говорит о несомненно благоприятном
влиянии применения Реамберина у больных с сосудистыми поражениями
головного мозга.
Таким образом, из приведенных данных видно, что у всех больных в
момент поступления в отделение реанимации имел место высокий
уровень эндотоксемии, введение препарата Реамберин позволяет
быстрее, чем в контрольной группе снизить уровень эндотоксикоза у
больных с сосудистыми поражениями головного мозга.
Как показано многочисленными исследователями (Safar, (1976);
Reves, (1990); Sidi, (1990); White, (1989); Scott, (1985); Dick,
(1992)) параметры ЭЭГ и их динамика коррелируют с уровнем мозгового
кровотока и определяются как состоянием кровотока, так и газовым
составом притекающей к мозгу крови, следовательно, анализ ЭЭГ
служит объективным критерием состояния кислородного баланса и
уровня метаболитов в мозге при различных патологических
воздействиях.
ДИНАМИКА СПЕКТРА ЭЭГ У БОЛЬНЫХ
С СОСУДИСТЫМИ ПОРАЖЕНИЯМИ ГОЛОВНОГО МОЗГА
(ПОСТИШЕМИЧЕСКИМИ
ЭНЦЕФАЛОПАТИЯМИ)
НА ФОНЕ ПРИМЕНЕНИЯ РЕАМБЕРИНА
В ходе клинического исследования выявлены некоторые особенности
состояния энцефалографический активности по данным нативной ЭЭГ и
при мониторировании ее спектра :
- У 22% больных на фоне применения Реамберина непосредственно в
ходе внутривенного капельного введения препарата и после окончания
введения препарата было отмечено нарастание амплитуды
энцефалограммы до 28% суммарной мощности от фоновой за счет
преимущественной активации частот дельта и тетта-диапазона;
- У 8% больных отмечено нарастание суммарной мощности спектра
ЭЭГ за счет активации частот альфа-диапазона, при этом нарастание
мощности спектра ЭЭГ сопровождалось активацией состояния
сознания до более высокого уровня (практически во всех случаях от
глубокого сопора до сопора или сонливости) на фоне применения
Реамберина или через 2-3 часа после окончания инфузии;
- У больных с фоновым уровнем сознания кома 3-4 и наиболее
грубой степенью депрессии энергетического метаболизма по данным
спектрограмм ЭЭГ (снижение вольтажа ниже 70-80% от стандартного)
выявлено наличие только медленно волновой части спектра и наличие
участков биоэлектрического молчания. Динамики спектрограмм на фоне
применения Реамберина не было, активации состояния сознания не
происходило, все больные погибли в ближайший период;
- Положительная динамика у 8% больных по данным КСА ЭЭГ и
уровню состояния сознания была отмечена в отсроченный период —
через 5-10 суток после окончания первого курса применения
препарата;
- Отрицательной динамики поданным КСА ЭЭГ, связанной с
применением Реамберина у больных ни в одном случае отмечено не было;
- Отрицательной динамики на уровень расстройств сознания
препарат не оказал ни в одном случае;
- Активация состояния сознания на фоне применения Реамберина у
больных с постгипоксической энцефалопатией имела место в 15%
случаев, что, учитывая фоновую глубину расстройств сознания, у
больных данной группы может считаться хорошим показателем;
- У 5% больных с тяжелыми поражениями мозга было отмечено
значительное увеличение сроков переживания (до 60 суток) по
сравнению с больными аналогичной тяжести, не получавшими
нейрометаболическую терапию Реамберином.
Положительная динамика, поданным спектрограмм при проведении
мониторинга ЭЭГ у больных с тяжелыми энцефалопатиями, активация
состояния сознания у части больных, увеличение сроков жизни
больных с тяжелейшими поражениями головного мозга, снижение
летальности больных указанных групп позволяют рекомендовать
использование препарата Реамберин в клинической реанимационной и
нейрореанимационной практике в качестве инфузионного
нейрометаболического корректора.
Таким образом, препарат Реамберин 1,5% для инфузнн
может быть рекомендован для терапии больных с сосудистыми
поражениями головного мозга при развитии синдрома полиорганной
недостаточности.
Применение Реамберина показано как для предоперационной
подготовки больных с сосудистыми поражениями головного мозга (при
геморрагическом инсульте, когда планируется хирургическое
вмешательство), так и для проведения интенсивной терапии в
послеоперационный период.
Препарат может быть использован в качестве корректора
характерных для больных с ишемическими и вторичными ишемическими
поражениями головного мозга при развитии синдрома полиорганной
недостаточности, расстройств энергометаболизма, что способствует
уменьшению выраженности эндотоксикоза, посгишемических поражений
как по клинико-лабораторным, так и по энцефалографическим
параметрам.
Применение препарата позволяет увеличить период жизни
пациентов и снизить уровень летальности больных с сосудистыми
поражениями голоного мозга даже при развитии синдрома полиорганной
недостаточности.
Применение препарата не вызывает аллергических реакций и
побочных действий.
Препарат может быть использован как комплексный
энергометаболит и корректор инфузионных расстройств у больных с
сосудистыми поражениями головного мозга как ишемического, так и
геморрагического характера в качестве средства выбора для
недифференцированной патогенетически обусловленной терапии.