А.Л. Коваленко, А.Ю. Петров, М.Г.Романцов
Биологическая активность экзогенного сукцината зависит от дозы,
режима введения препарата, его химической формы (кислота, соль,
сложный эфир) и функционального состояния организма.
При применении физиологических доз янтарной кислоты можно
выделить две группы эффектов:
- прямое действие ЯК на клеточный метаболизм,
- влияние ЯК на транспорт свободного кислорода в ткани.
Добавление небольших количеств фумарата, малата или сукцината к
суспензии измельченной мышечной ткани приводит к приросту
потребления тканью кислорода, многократно большему, чем можно было
бы объяснить только окислением добавленных субстратов до диоксида
углерода и воды.
Процесс носит каталитический характер, поскольку одна молекула
добавленной к ткани дикарбоновой кислоты обеспечивает окисление
многих эндогенных субстратов. Однако, стимулирующее действие
какой-либо из названных карбоновых кислот на потребление
кислорода отменяется ингибитором сукцинат дегидрогеназы (СДГ) –
малонатом. Иными словами, окисление сукцината является необходимым
условием каталитического действия любой другой из карбоновых кислот
на усвоение тканью кислорода.
Этот феномен был объяснен Кребсом, который показал, что
последовательность реакции окисления ряда три- и дикарбоновых
кислот замкнуты в цикл, позже названный его именем. Для поддержания
нормального тканевого дыхания теоретически достаточно лишь
активированной уксусной кислоты (ацетил-КоА), а другие субстраты не
расходуются.
Однако в действительности ди- и трикарбоновые кислоты постоянно
отвлекаются из цикла Кребса в качестве субстратов анаболических
реакций.
Потеря интермедиатов цикла возрастает при острых и хронических
отравлениях аммиаком. Пополнение пула кислот цикла Кребса
нарушается при алкоголизме, гиповитаминозе В и при отравлениях
ингибиторами пиридоксальфосфат зависимых ферментов. Поэтому
пополнение пула интермедиатов цикла Кребса, в том числе и из
пищевых источников, является необходимым. Для пополнения пула всех
органических кислот цикла Кребса оказалось достаточным экзогенного
введения лишь одного сукцината
Сукцинат является стимулятором синтеза восстановительных
эквивалентов в клетке. Феномен быстрого окисления сукцината в
цитоплазме клеток, сопровождающийся восстановлением пула
динуклеотидов, отмечаемый при внесении избытка ЯК, получил название
- "монополизация дыхательной цепи сукцинатом". Биологическое
значение данного явления заключается в быстром ресинтезе клетками
АТФ и в повышении их антиоксидантной резистентности.
Кроме того, сукцинат положительно влияет на оксигенацию
внутренней среды, стабилизирует структуру и функциональную
активность митохондрий, являясь индуктором синтеза некоторых
белков, влияя на ионный обмен в клетке.
Введение здоровым людям или лабораторным животным сукцината
натрия приводит к снижению уровня органических кислот в крови и
экскреции кислых продуктов обмена из организма (частично – в виде
аммонийных солей), что указывает на нормализацию аэробной фазы
тканевого дыхания.
Преимущества сукцината в скорости окисления перед другими
субстратами клеточного дыхания наиболее выражено в условиях
гипоксии, когда НАД-зависимый транспорт электронов в дыхательной
цепи тормозится, а активность СДГ и продукции эндогенного сукцината
возрастает.
Способность экзогенной янтарной кислоты существенно
интенсифицировать диффузию кислорода в клетке различных тканей in
vitro свидетельствует о возможном повышении сукцинатом
трансмембранного градиента концентрации кислорода и,
соответственно, снижения оксигенации ядра и цитоплазмы.
Исследования показали наличие у янтарной кислоты биологической
активности с уникальным сочетанием проявлений: по отношению к
здоровому организму сукцинаты выступают в роли адаптагенов и
актопротекторов, а при наличии патологических проявлений проявляют
нетипично высокий для адаптагенов терапевтический эффект. Особенно
перспективно лечебное применение сукцинатов при заболеваниях
сердечно-сосудистой (острая и хроническая ишемическая болезнь
сердца), дыхательной, эндокринной систем, при желудочно-секреторной
недостаточности и поражениях печени различной этиологии,
онкологических, психических заболеваниях, в качестве стимуляторов
посттравматической регенерации.
С профилактической целью янтарная кислота используется в
спортивной медицине, для профилактики состояния пониженной
иммунологической реактивности и для повышения устойчивости к
неэлектролитному действию алкоголя. Перспективно ее применение для
формирования статуса повышенной резистентности организма к
ионизирующим излучениям, алкилирующим ядам и биологическим
агентам.
В основе лечебно-профилактических свойств янтарной кислоты и ее
соединений лежит модифицирующее влияние на процессы тканевого
метаболизма - клеточное дыхание, ионный транспорт, синтез белков.
При этом амплитуда и направленность модификаций зависят от
исходного функционального состояния тканей, а ее конечный результат
выражается в оптимизации параметров их функционирования.
Такие свойства позволяют отнести сукцинаты к
лечебно-профилактическим препаратам нового поколения - так
называемым "умным лекарствам".
Учитывая уникальную разносторонность проявлений биологической
активности ЯК, сфера ее применения в медицинской практике является
пока еще - чрезмерно узкой. Поэтому направление по созданию
препаратов на основе ЯК является весьма перспективным.
Янтарная кислота (рис. 1) и е. соли и эфиры - сукцинаты
представляют собой универсальный внутриклеточный метаболит, широко
участвующий в обменных реакциях в организме, являясь малотоксичным
соединением и не обладает мутагенным и тератогенным действием.
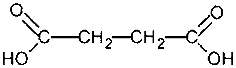
Рис. 1. Янтарная кислота
Содержание ЯК в тканях организма человека и животных, составляет
0.2-0.8 ммоль/кг, а ее концентрация в плазме крови значительно
меньше и не превышает 0.04 ммоль/л.
Окисление ЯК в шестой реакции цикла Кребса осуществляется с
помощью специфического фермента - сукцинат дегидрогеназы,
характерной особенностью которой является локализация на внутренней
мембране митохондрий и независимость е. активности от концентраций
окисленной и восстановленной форм НАДН+/НАД, что позволяет
сохранить энергосинтезирующую функцию митохондрий в условиях
гипоксии при нарушении НАД-зависимого дыхания клеток; выполняя
каталитическую функцию по отношению к циклу Кребса ЯК снижает
концентрацию в крови других интермедиатов цикла - лактата, пирувата
и цитрата, накапливающихся в клетках на ранних стадиях
гипоксии.
В нервной ткани функционирует, так называемый g-аминобутирантный
шунт (цикл Робертса), в ходе которого ЯК образуется из
g-аминомаслянной кислоты через промежуточную стадию янтарного
альдегида. Следует заметить, что в условиях стресса и гипоксии
органов и тканей образование ЯК возможно в реакции окислительного
дезаминирования a-кетоглутаровой кислоты в печени .
ЯК в организме нормализует содержание гистамина и серотонина в
крови и повышает микроциркуляцию в органах и тканях, не оказывая
влияния на артериальное давление и показатели работы сердца.
Экспериментально показано при остром инфаркте миокарда в крови,
вытекающей из зоны ишемии, происходит резкое уменьшение содержания
ЯК, усугубляя гипоксию миокарда. Экзогенное поступление в организм
ЯК нормализует активность сукцинат дегидрогеназы, ограничивает зону
некроза в миокарде, при этом усиливается биоэлектрическая
активность сердца (под действием ЯК), улучшается гемодинамика и
увеличивается толерантность сердца к физическим нагрузкам.
Противоишемический эффект ЯК связан не только с активацией
сукцинат дегидрогеназного окисления, но и с восстановлением
активности ключевого окислительно-восстановительного фермента
дыхательной цепи митохондрий клеток - цитохромоксидазы.
Антиаритмическое действие ЯК обусловлено улучшением
метаболических процессов в миокарде, подавлением процессов
перекисного окисления липидов в кровотоке и стабилизацией
коронарного кровоснабжения. Потенцирующее действие ЯК на
противоаритмическую эффективность новокаинамида обусловлено, помимо
влияния на метаболические процессы в миокарде, влиянием на
калиевый/кальциевый обмен в кардиомиоцитах. Кардиопротекторное
действие ЯК связано с активацией сукцинат дегидрогеназного пути
окислительного ресинтеза АТФ в кардиомиоцитах, с одновременным
снижением уровня жирных кислот и НАД-зависимых субстратов цикла
Кребса в зоне ишемии.
В условиях экспериментального шока, вызванного 10-минутной
остановкой сердца, ЯК снижала уровень свободнорадикальных процессов
в мозге и сыворотке крови, ослабляла деструкцию мембраных элементов
нейронов и способствовала полному восстановлению функций и
структуры мозга. В постреанимационном периоде ЯК способствовала
нормализации функций центральной нервной системы, снижала
чувствительность животных к стрессу, накопление
свободно-радикальных продуктов и восстанавливала морфологические
изменения в крови и головном мозге. Избирательное действие ЯК на
гипоталамические структуры мозга позволяет усиливать действие
эстрогенов на гормонозависимые органы и ткани.
При экспериментальном шоке, вызванном массивной кровопотерей ЯК
повышала выживаемость животных и восстанавливала функциональную
активность почек; способствовала растворению камней при
экспериментальном уролитиазе, подавляя синтез оксалатов.
При экспериментальной острой гипоксии мозга ЯК ограничивала
объем ишемических повреждений, уменьшала количество продуктов
перекисного окисления липидов и увеличивала выживаемость
животных.
Повышение трансмембранного градиента концентрации кислорода и
снижение оксигенации ядра и цитоплазмы кислорода свидетельствует о
способности ЯК интенсифицировать диффузию кислорода в различные
ткани и органы, стимулируя при этом клеточное дыхание: так, прирост
скорости потребления кислорода клетками печени при добавлении ЯК
увеличивается в 60 раз. Способность ЯК интенсифицировать утилизацию
кислорода тканями и восстановление НАД-зависимого клеточного
дыхания характеризуют е. антигипоксическое действие.
Восстановление пула пиримидиновых динуклеотидов приводит к
увеличению концентрации восстановленного глутатиона и усилению
устойчивости митохондрий к перекисной деградации, стимулированной
ксенобиотиками, при этом , ЯК под действием сублетальных доз
активного генератора радикальных частиц - нитрита натрия полностью
нивелирует блокирование дыхательной цепи митохондрий.
Гепатотропное действие ЯК обусловлено повышением соотношения
НАДН+/НАД, стимуляцией синтеза мочевины и энергетического обмена в
гепатоцитах. Активация сукцинат дегидрогеназы в митохондриях
гепатоцитов под действием ЯК нормализует печеночный холестаз и
препятствует жировой дистрофии печени и образованию коллагенозной
ткани. При поражении печени ксенобиотиками ЯК стимулирует ее
метаболизирующую функцию с одновременным повышением устойчивости
мембран гепатоцитов к радикальному окислению.
Несмотря на известные фармакологические эффекты ЯК,
зарегистрированных лекарственных форм, содержащих в качестве
основного компонента ЯК, немного.
В составе комплексных лекарственных препаратов, ЯК потенцирует
фармакологические эффекты многих активных субстанций
(антигипоксическую активность 1, 2, 4-тиадиазола). Высокая
алкопротекторная активность ЯК реализована в таблетках "Лимонтар",
содержащих комбинацию янтарной и лимонной кислот и в
антиоксидантном препарате "Мексидол".
Комбинация ЯК с ацетилсалициловой кислотой предложена в качестве
противоспалительного, а сорбитом (ксилитом) в качестве
противодиабетического лекарственного средства. В качестве
противоастматического средства и бронходилататора разработана
комбинация ЯК с сальбутамолом.
Исследователями (Галенко-Ярошевский с соавт., 1998; Малюк В.И. с
соавт., 1981; Морозова К.И., 1990) показана стимуляция
мерцательного эпителия бронхов, нормализация состава
бронхолегочного лаважа и функциональной активности альвеолярных
макрофагов, под воздействием ЯК, при бронхолегочной патологии.
Таким образом, ЯК являясь фармакологически высоко активным
соединением может быть использована для получения новых
лекарственных препаратов с улучшенными фармакологическими
свойствами.
Высокая антигипоксическая и антиоксидантная активность ЯК нашла
применение в дезинтоксикационном растворе "Реамберин 1,5% для
инфузий" в состав которого входят: активное вещество - смешанная
натрий N-метил-глюкаминовая соль янтарной кислоты, микроэлементы в
оптимальных концентрациях.
Препарат разрешен ФГК МЗ РФ к клиническому применению и показан
при экзо- и эндогенных интоксикациях.
Как показали экспериментальные исследования на животных при
изучении обще токсического действия на доклиническом этапе изучения
препарата Реамберин в остром, подостром и хроническом эксперименте
продемонстрировано, что во всех исследуемых дозах не выявлено
патологических сдвигов со стороны основных жизненно важных функций
органов и систем; также установлено, что препарат не вызывает
дистрофических, деструктивных, очаговых склеротических изменений в
паренхиме и строме изучаемых органов; не отмечено
местно-раздражающего действия препарата при внутривенном способе
введения.
При изучении подострой и хронической токсичности показано, что
препарат не оказывает токсического воздействия на функционирование
сердечно - сосудистой системы, на морфологический состав и
биохимические показатели периферической крови и костного мозга, на
функциональное состояние печени, почек, а также на белковый,
углеводный, жировой и электролитный виды обмена веществ.
Результаты доклинического исследования, проведенного в
соответствии с утвержденным Фармакологическим Комитетом МЗ РФ
протоколом изучения обще токсического действия препарата Реамберин,
позволяют заключить, что он относится к 5 классу практически
нетоксичных лекарственных средств, является безопасным и безвредным
препаратом, что позволило разрешить его применение в клинической
практике.
На основании полученных данных можно заключить, что препарат
Реамберин удовлетворительно переносится и не приводит к развитию
осложнений и побочных эффектов при его пролонгированном
использовании.
Исследования проводились на основании решения ГФК МЗ РФ "О
разрешении клинических испытаний Реамберина 1,5% для инфузий" в
качестве метаболического средства при интоксикациях различного
генеза (протокол N11 от 30.12.99)."
Таким образом, Реамберин препарат, содержащий натрия сукцинат,
магния хлорид, калия хлорид, натрия хлорид, обладающий
дезинтоксикационным, антигипоксическим, антиоксидантным, гепато,
нефро и кардиопротекторным действием. Основной фармакологический
эффект препарата обусловлен способностью усиливать компенсаторную
активацию аэробного гликолиза, снижать степень угнетения
окислительных процессов в цикле Кребса в дыхательной цепи
митохондрий клеток с увеличением внутриклеточного фонда
макроэнергетических соединений аденозинтрифосфата (АТФ) и
креатинфосфата.
Реамберин активирует антиоксидантную систему ферментов и
тормозит процессы перекисного окисления липидов в ишемизированных
органах, оказывая мембраностабилизирующее действие на клетки
головного мозга, миокарда, печени и почек. Препарат способствует
процессам репаративной регенерации гепатоцитов, что проявляется
снижением уровня в крови маркерных ферментов поражения ткани
печени.
Показания:
- Интоксикации различной этиологии: отравление ксенобиотиками,
инфекционно-токсический шок, лекарственные, токсические и
холестатические гепатиты, желтушные формы вирусных гепатитов;
- Гипоксические состояния различного генеза: искусственный наркоз,
ранний постоперационный период, массивная кровопотеря, острая
сердечная и дыхательная недостаточность и другие нарушения
кровообращения органов и тканей.