Сегодня на фармацевтическом рынке Росӯсии представлено большое количество средств метаболической направленности действия, коӯторые в зарубежной медицинской литературе определяются как “модификаторы биологичесӯкого ответа”. Основной проблемой в применеӯнии их в клиниӯческой практике является отӯсутствие доказательных режимов дозироӯвания при каждой конкретной патологии и у каждого конкретного пациӯента. Эта проблема связана как с отстутствием многоцентровых рандомиӯзированных исследований эффективности и беӯзопасности применения данной группы лекарсӯтвенных средств, так и разработанной технолоӯгической платформы для проведения фармако-кинетических исследований и оценки фармакодина мических эффектов на молекуӯлярном уровне.
В настоящем исследовании (на примере поӯпуляции пациентов с сахарӯным диабетом (СД) тип 1, находящихся в стадии декомпенсации) разраӯботана схема оценки фармакодинамических эффектов и предложена новая методика оценки фармакокинетических показателей инфузионной среды «Реамберин 1,5% для инфузий» в состав которой входит активное вещестӯво – смешанная натрий N-метилглютаминовая соль янтарной кислоӯты, электроӯлиты в оптиӯмальных для солевого кровезаменителя конӯцентрациях.
СД относится к распространенным заболеӯваниям. Им страдает около 3-4% населения. Ожидаемая распространенность СД к 2010 году составит около 215 млн человек [1]. СД тип 1 составляет 15-20% от всех больных диабетом. В настоящее время, несмотря на появляющиеся эпидемиоӯлогиӯческие данные и результаты мноӯгоцентровых исследований, свидетельӯствуюӯщих о наличии патогенетической взаимосвязи между метаболиӯческими расстройствами при СД и его осложнениями, современные клиӯниӯӯческие руководства и международные рекоменӯдации не уделяют достаӯточного внимания ноӯвым методам лечения СД, эффективно воздейсӯтвующим на метаболомные процессы. В связи с интенсивным развитием новых знаний в обласӯти геномики, транскриптомики, метаболомики станоӯвятся возможными разработка и применеӯние лекарственных средств с целенаправленӯным воздействием на молекулярные процессы, происхоӯдящие на уровне клетки при СД. СД соӯпровождается структурными измеӯнениями сосудов и ткани почек, сердца, головного мозга. В основе этих изменений лежит энергодефицит, нарушение ресинтеза белка, фосфоӯлипидов и других структурных компонентов клетки, акӯтивация своӯбодноӯрадикального окисления. Дискуссионным остается вопрос, касаюӯщийся применения лекарственных средств, обладаюӯщих метаболическим действием и способствуюӯщих улучшению нейронального метаболизма, стабилизации физиологических механизмов ауторегуляции мозгового, кардиального и поӯчечного кровообращения, которые нарушены в условиях энергетического дисбаланса при СД тип 1.
Цель работы – разработка нового подхода к индивидуализации дозирования лекарственӯных средств с метаболической направленносӯтью действия у пациентов с СД тип 1 на примере инфузионной среды «Реамберин 1,5% раствор для инфузий» в условиях клинико-фармаколоӯгического исследования с разработкой новых методов оценки регуляции и функционироваӯния метаболических шунтов, связанных с проӯдукцией и трансформацией янтарной кислоты.
Материал и методы
Настоящее исследование являлось проӯспективным сравнительным с параллельным дизайном. В исследование было включено 36 пациӯентов с СД тип 1, находившихся в ста дии декомпенсации, согласно клинико-анамӯнестической характеристике, представленной в таблице 1. Контрольную группу пациентов соӯставили 17 человек, принимавших интенсифиӯцированный режим инсулинотерапии (ИИ), исследуемую группу – 19 человек, получавших ИИ и Реамберин 1,5% раствор, внутриӯвенно ка пельно, со скоростью 60 капель в минуту, 400 мл, в 17.00, через 48 часов, количество внутривенных введений ӯ 5. Категория пациенӯтов с СД тип 1 соответствовала критериям СД тип 1 подтип Б, отлиӯчающегося от пациентов с СД тип 1 подтип А длительностью заболевания к моменту появления потребности в инсулине (не превышает 3-4 лет). Конечной точкой исӯследования являлись критерии компенсации СД [2]. В стадии декомпенсации больной полуӯчал ИИ, включавшую введение инсулина коӯроткого действия (Хумулин R, Eli Lilly, США) и инсулина продленного действия дважды в день (вместо базальной секреции, Хумулин Н, Eli Lilly, США). Доза инсулина короткого действия опредеӯлялась из расчета 1 ЕД на каждые 1,7 ммоль/л. постпрандиальной гликемии выше 7,8 ммоль/л. Инсулин средней продолжительӯности действия назначался в начальной дозе из расчета 0,2-0,5 Ед/кг веса и корригировался по уровню гликемии: натощак 1 ЕД инсулина на каждые 1,1 ммоль/л, превышающие 7,7 ммоль/л.
Таблица 1. Клинико-анамнестическая характеристика пациентов
|
Показатель |
Целевая популяция (выборка) |
|
Пол (мужчины/женщины) |
12/24 |
|
Возраст, годы: I возрастная группа (до 25 лет), кол. II возрастная группа (до 30 лет), кол. III возрастная группа (до 50 лет), кол. |
8 22 6 |
|
Масса тела, кг |
68,2ұ3,7 |
|
Индекс массы тела, кг/см2 |
25,5ұ1,1 |
|
Рост, см |
170,3ұ3,3 |
|
Длительность диабета, годы |
7,8ұ2,3 |
|
Длительность АГ годы: I ст. II ст. III ст. |
3,2ұ1,8 6,8ұ1,2 9,8ұ1,6 |
|
Длительность приема инсулина, годы |
5,7ұ1,1 |
|
Сроки возникновения потребности в инсулине, годы |
2,4ұ0,5 |
|
Диабетическая нефропатия: стадия начинающейся диабетической нефропатией (III стадия), кол. |
27 |
|
ХСН, ФК, кол.: ФК I класс |
15 |
|
Диабетическая нейропатия, кол. |
18 |
Для оценки влияния Реамберина на фоне ИИ на глюкодинамику у больных определяли содержание глюкозы натощак и в 9.00, 13.00, 17.00 (гликемический профиль больного) на биохимическом диализаторе BioStat Fax+ (США). Для оценки характера изменений конӯцентрации глюкозы испольӯзовались критерии диагностики СД и других нарушений толерантӯности к глюкозе, предложенных американской ассоциацией диабета. Определялся уровень НbА1c, являвшийся косвенным подтверждениӯем наличия метаболического эффекта у Реамбеӯрина на фоне ИИ. Нормальный уровень НbА1c не превышал 8,3%. О степени компенсации угӯлеводного обмена в процессе лечения инсулиӯном и Реамберином судили по следующим покаӯзателям HbA1c: HbA1c до 9% – хорошая комӯпенсация; HbA1c 9-10 – удовлетворительная компенсация; HbAlc более 10% – плохая комӯпенсация. Концентрация креатин и на определяӯлась кинетиӯческим методом по реакции Яффе. Регистрировались уровнь адреноӯкортикотропного гормона (АКТГ), кортизола, иммунореактивного инсулина (ИРИ), тиреотропного гормоӯна (ТТГ), тироксина (T4), трийодтиронина (Т3) методом радиоиммунологического анализа (РИА). Концентрация глутамата в сывротке крови определялась с целью анализа роли янтарной кислоты в реализации активности глутамата в организме пациентов с СД тип 1 на фоӯне приема Реамберина (биохимический аналиӯзатор BioStat Fax+, США). Для оценки активӯности ПОЛ определяли содержание МДА по реакции с ТБК в кислой среде. Норма составляӯет 3,4-6,8 мкмоль/л. Определение активности СОД основано на способности фермента подавӯлять реакцию восстановления нитросинего тетраӯзолия супероксидным анион радикалом, геӯнерированным in vitro в системе ксантин: ксантиноксидаза. Динамика содержания Na+, K+, Са ++, Mg++в сыворотке крови больных СД тип 1 оценивалась методом пламенной спектроӯфотометрии. Определение ионов хлора в сыворотӯке крови выполнялось меркуриӯметрическим методом с индикатором дифенилкарбазоном. Регистриӯровали степень протеинурии и уровень креатинина в моче. Применялась методика S. M. Marshallв оценке соотношения альбумин/креатинин мочи (ДСА - 2000, «Вауеr». [3, 4, 5].
В настоящее время разрабатывается техноӯлогическая платформа для фармакокинетического анализа Реамберина на основе концентраӯций янтарной кислоты (уровня концентрации янтарной кислоты в крови пациента до назначеӯния и на фоне приема Реамберина) в биологиӯческих жидкостях у данного контингента больӯных. В программе ADAPT II рассчитываются индивидуальные значения оптимальных моӯментов измерений концентрации сукцината в крови в популяции пациентов с СД тип 1.
В качестве внутреннего стандарта применяӯлась янтарная кислота (сукцинат, Sigma Aldrich, Германия).
Условия LC/MS-анализа . Электроспрейная ионизация (ESI), скорость поӯтока через колонку 1,5 мл/мин, температура геӯнератора азота 3500әС со скоростью потока азоӯта 12 л/мин, давление распылителя 172 кПа, хроматографическая колонка Hypersil Amino Acid(5јm, 250x4,6 mm), температура на колонӯке подвижные фазы ацетонитрил: аммония ацеӯтат (Sigma Aldrich) (70:30 от объема соответсӯтвенно). Диапазон m/zсоставляет 50-200. Ввоӯдимый объем образца 5 мкл.
Качество жизни (КЖ) пациентов оцениваӯли по опроснику theDiabetes Quality of Life (низкий бал – дискомфорт и беспокойство, выӯсокий – удовлетворительное КЖ). Длительӯность исследования составила 1 месяц.
Первичную и вторичную статистическую обработку материала исследования проводили на персональном IBM совместимом компьютере с процессором Pentium IV с использованием паӯкета статистических программ для биомедиӯцинских исследований «Statisticа 6.0». В клиническом исследовании определялись следуюӯщие параметры описательной статистики; средӯняя (М), стандартная ошибка средней (SEM), t-критерий Стъюдента. Проводилась оценка норӯмальности распределения полученных данных.
Результаты и их обсуждение
В контӯрольной группе пациентов отмечено достоверӯное снижение среднесуточного, максимального уровней глюкозы при отсутствии достоӯверных изменений ее минимального уровня и уровня HbA1c, конценӯтрации МДА в крови, скорости образования сопряженных диенов и концентраӯции глутаминовой кислоты в крови. Зарегистӯрировано значиӯмое увеличение уровня СОД в крови и продолжительности лаг-периода (табл. 2).
Таблица 2. Динамика показателей гликемии, глутамата и активности продуктов ПОЛ в крови пациентов СД тип 1 (контрольная группа)
|
Параметры |
Исходно |
через месяц |
|
Глюкоза плазмы, ммоль/л среднесуточный уровень максимальный уровень минимальный уровень |
9,3ұ3,9 13,5ұ3,4 4,6ұ1,4 |
6.53ұ0,6*** 10,2ұ0,3*** 4,6ұ0,3` |
|
HbAlc, % |
10,3ұ0,7 |
9,3ұ0,3` |
|
Концентрация МДА, мкмоль/л |
1.8ұ0,03 |
1,7ұ0,05` |
|
Лаг-период (мин) |
55,3ұ2,4 |
60,8ұ1,8* |
|
Скорость образования сопряженных диенов, нмоль х л-1 х мин-1 |
17,6ұ0,3 |
17,1ұ0,5` |
|
СОД, усл. ед. |
1,2ұ0,1 |
1,5ұ0,1** |
|
Глутаминовая кислота, мкмоль/л |
37,3ұ2,7 |
38,9ұ4,0` |
` – недостоверные различия; * – р < 0,05; ** – р<0,01; *** – р<0,001
Применение Реамберина приводило к достоӯверному снижению среднесуточного, максиӯмального и минимального уровней глюкозы, HbA1с концентрации МДА, уменьшению проӯдолжительности лаг-периода и скорости образоӯвания ДК с увеличением СОД и содержания глуӯтаминовой кислоты в крови (табл. 3).
Таблица 3. Динамика показателей гликемии, глутамата и активности продуктов ПОЛ в крови пациентов СД тип 1 на фоне приема ИИ и Реамберина
|
Параметры |
Исходно |
Через месяц |
|
Глюкоза плазмы, ммоль/л среднесуточный уровень максимальный уровень минимальный уровень |
9,94ұ0,48 14,07ұ1,55 4,98ұ0,78 |
5,48ұ0,59*** 8,59ұ0,58*** 4,18ұ0,35` |
|
HbAlc, % |
10,21ұ0,40 |
8,11ұ0,38*** |
|
Концентрация МДА, мкмоль/л |
1,79ұ0,079 |
1,55ұ0,036*** |
|
Лаг-период (мин) |
56,39ұ1,92 |
61,39ұ1,76*** |
|
Скорость образования сопряженных диенов, нмоль х л-1 х мин-1 |
17,77ұ0,43 |
16,38ұ0,15** |
|
СОД, усл. ед. |
1,12ұ0,095 |
1,44ұ0,058*** |
|
Глутаминовая кислота, мкмоль/л |
34,21ұ3,33 |
68,2ұ2,34*** |
` – недостоверные различия; * – р < 0,05; ** – р<0,01; *** – р<0,001
Таблица 4. Динамика показателей протеинурии и уровня креатинина в сыворотке крови у пациентов контрольной группы
|
Параметры |
Исходно |
Через месяц |
|
Креатинин, мкмоль/л Протеинурия, г/сут |
103,5ұ8,6 1,6ұ0,1 |
96,7ұ3,7` 1,5ұ0,1` |
` – недостоверные различия; * – р < 0,05; ** – р<0,01; *** – р<0,001
Таблица 5. Динамика показателей протеинурии и уровня креатинина в сыворотке крови у пациентов с СД тип 1 на фоне приема ИИ и Реамберина
|
Параметры |
Исходно |
Через месяц MұSEM |
|
Креатинин, мкмоль/л Протеинурия, г/сут |
106,4ұ4,6 1,6ұ0,02 |
72,3ұ3,0*** 0,4ұ0,2*** |
` – недостоверные различия; * – р < 0,05; ** – р<0,01; *** – р<0,001
Таблица 6. Оценка микроальбуминурии по соотношению альбумин/креатинин
мочи
в контрольной и исследуемой группах пациентов с СД тип 1
|
Режимы фармакотерапии |
Альбумин/креатинин мочи (мг/ммоль) |
|
ИИ |
|
|
исходно |
12,4ұ0,3 |
|
через месяц |
12,1ұ0,2` |
|
ИИ + Реамберин |
|
|
исходно |
12,1ұ0,2 |
|
через месяц |
4,7ұ0,1*** |
` – недостоверные различия; * – р < 0,05; ** – р<0,01; *** – р<0,001
В контрольной группе пациентов с СД тип 1 и в исследуемой группе обнаружены микро-, макроальбуминурия и протеинурия, при этом уроӯвень креатинина сыворотки крови находился на верхней границе нормальных значений (табл. 4, 5). Применение Peaмберина сопровождалось достоверным уменьшением выраженности протеиӯнурии, при статистически значимом снижении концентрации креатинина в сыворотке крови в пределах нормальных значений по сравнению с контрольной группой (таблица 5). В контрольной группе пациентов выявлено увеличение коэфӯфициента альбуӯминурия/креатинин мочи > 10 мг/ммоль, что свидетельствовало о существоӯваӯнии стабильной микроальбуминурии (таблица 6). В группе больных, принимавших Реамберин зарегистрировано статистически достоверное устӯранение микроальбуминурии с последующим снижением отношения альбумин/креатинин моӯчи (табл. 6).
В контрольной группе отмечено достоверӯное уменьшение концентраӯции ионов Na+, иоӯнов хлора в сыворотке крови при увеличении содерӯжания ионов Са++ и соотношения Na+/K+ (табл. 7). В группе пациентов, получавших ИИ и Реамберин, отмечалось достоверное и более выраженное уменьшение ионов Na+, K+ и хлора в сыворотке крови при значимом увеличении соотношения Na+/K+, Mg++ и Са++ в сыворотке крови (табл. 8).
Таблица 7. Изменение параметров электролитного баланса
у пациентов с СД тип 1 (контрольная группа)
|
Параметры |
Исходно |
Через месяц |
|
Na+, ммоль/л |
155,7ұ2,3 |
147,9ұ3,8* |
|
K+, ммоль/л |
5,0ұ0,4 |
4,5ұ0,2` |
|
Na+/K+ |
30,2ұ2,2 |
32,5ұ1,9* |
|
Mg++, мкмоль/л |
0,5ұ0,05 |
0,51ұ0,1` |
|
Cl+, ммоль/л |
107,8ұ2,7 |
98,2ұ3,7* |
|
Са ++, ммоль/л |
`2,2ұ0,1 |
2,5ұ0,1* |
` – недостоверные различия; * – р < 0,05; ** – р<0,01; *** – р<0,001
Таблица 8. Изменение параметров электролитного баланса у пациентов с СД тип
1
на фоне приема ИИ и Реамберина
|
Параметры |
Исходно |
Через месяц |
|
Na+, ммоль/л |
154,9ұ2,5 |
139,8ұ3,5*** |
|
K+, ммоль/л |
5,0ұ0,3 |
3,9ұ0,3*** |
|
Na+/K+ |
29,7ұ1,9 |
35,7ұ1,4*** |
|
Mg++, мкмоль/л |
0,5ұ0,05 |
0,8ұ0,04*** |
|
Cl+, ммоль/л |
106,3ұ2,6 |
97,3ұ2,9*** |
|
Са ++, ммоль/л |
2,3ұ0,1 |
2,5ұ0,03** |
` – недостоверные различия; * – р < 0,05; ** – р<0,01; *** – р<0,001
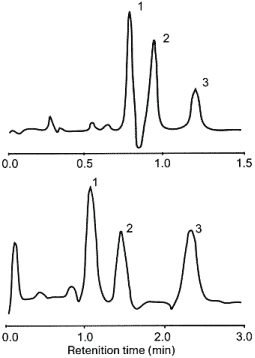
Рис. 1. Хромато-масс-спектрометрические пики:
1-гомоцистеин; 2-метилмалоновая кислота
Анализ результатов исследований содержания гормонов гипофиӯзарно-надпочечниковой оси, оси гипофиз-щитовидная железа и инсуӯлина в течение суток в состоянии покоя, а также АКТГ у пациентов с СД тип 1, обнаружил, что уровни этих гормонов значительно выше, чем вечерние, за исключением ТТГ (табл. 9, 10). Сравнительный анализ содерӯжаӯния гормонов в крови пациентов контрольной группы продемонӯстрировал следующие закономерности
У больных, принимавших Реамберин, значительӯно уменьшался процент лиц с неудовлетвориӯтельным КЖ и увеличивалось количество пациӯентов с удовлетворительным КЖ по шкале the Diabetes Quality of Life по сравнению с контӯрольной группой пациентов.
В ходе исследования обнаружен высокий терапевтический эффект янтарной кислоты («Реамберин 1,5% для инфузий»), связанный с гормонально-метаболическим (обменномодифицирующим) и антиоксидантным действием вещества. Как известно, основной причиной поӯражения органов-мишеней (сердце, головной мозг, почки, глазное дно) при СД тип 1 является поражение сосудов этих органов. Основная роль в развитии сосудистых осложнений СД принаӯдлежит неферментативному аутоокислительному гликозилированию и окислительному стресӯсу. При терапии Реамберином, вероятно, увелиӯчивается чувствительность инсулиновых реӯцепторов к инсулину и уменьшается гипергликемия, что устраняет механизмы акӯтивации окислительного стресса. Увеличение чувствительности к экзогенному инсулину моӯжет быть связано с положительным действием сукцината на оксигенацию внутриклеточной среды, стабилизацию структуры и функции миӯтохондрий, ионный обмен в клетке, о чем косвенно могут свидетельствовать внеклеточные изменения Na+/K+, Ca++, хлора, Mg++. Обнаруӯжены сопряженные изменения функционироӯвания оси гипофиз-надпочечники и системы ПОЛ-АОС на фоне приема Реамберина. Наибоӯлее вероятной мишенью представляются глюкокортикоидные рецепторы II и III типа. Мехаӯнизм их ингибирования (концепция G. Vailette) может быть связан со взаимодействием со втоӯрым неспецифическим локусом, расположенӯным вне пределов специфического глюкокортикоидного локуса глюкокортиӯкоидного рецептоӯра II и III типа, что вызывает трансформацию специфического глюкокортикоидного локуса, которая является причиной снижения глюко-кортикоидсвязывающей способности рецептоӯра II и III типа. В конечном итоге, снижается уровень активности Са++-кальмодулинзависимой NО-синтазы с восӯстаӯновлением физиологиӯческого уровня N0. Возможными механизмами реалиӯзации кардио- и вазопротективного эфӯфекта Реамберина у пациентов с СД тип 1 являются:
- устранение неблагоприятных эффектов гипергликемии – угнетение активӯности гликозилирования, пероксидации белков и радикала N0;
- влияние на биохимические процессы – бета-окисление жирных кислот, окислительное фосфорилирование глюкозы в миокарде, синтез АТФ, синтез коллагена в серӯдце;
- опосредованное изменение уровня функӯционирования нейроэндокринӯной регуляции (инсулин, кортизол, Т3).
Достоверное уменьшение активности ПОЛ и снижение концентрации НbА1су пациентов с СД тип 1 в ходе приема Реамберина может свиӯдетельӯствовать о снижении образования проӯдуктов неферментативного гликозилиӯрования белков-оснований Шиффа (обратимых), слабо обратимых (продуктов Амадори) и необратиӯмых конечных продуктов гликозилирования. На уровне нефроцита представляется вероятӯным возникновение на фоне приема Реамберина явления адаптационного резерва, который свяӯзан с активностью глуӯтаматдегидрогеназного комплекса: происходит снижение активности глутаӯматӯдегидрогеназы, что может быть вызваӯно увеличением содержания NAD·H2 в резульӯтате торможения активности ферментов NAD·H-дегидрогеназы и цитоӯхромоксидазы в митохондриях почек. Возможно накопление пиридиннуклеоӯтида за счет генетически опосредованного синтеза, являющегося аллостериӯческим регулятором глутаматдегидрогеназы, что обращает ферментативную реакцию в стоӯрону образования глутаминовой кислоты, которая способна связать аммиак в этот период. Другим важным следствием обращения этой реӯакции является генерирование окисленного NAD, наличие которого обеспеӯчивает возможӯность катализа дегидрирования субстратов. На уровне нефроцита происходит убывание глутамата в цикле Робертса, что способствует предохӯранению сукцинатдегидрогеназы от ингибирующего действия оксалоацетата и обеспечивает достаточно высокий уровень энергопродукции для клеток органа. Увеличение окисления глутамата может приводить к шунтированию α-кетоӯглутарата с преобразовнием последнего в цикле Кребса. Наблюдающаяся актиӯвация глиӯколиза является одним из механизмов, способсӯтвующих поддержанию уровня АТФ, а также служит поставщиком субстратов окисления для цикла Кребса. С другой стороны, не исключен рост глутаминсинтетазы, что может споӯсобӯствоӯвать накоплению N-ацетилглутамата, активиӯрующего карбомоилӯсинтетазу.
Механизмами антиоксидантного эффекта Реамберина в отношении нейронов головного мозга являются:
- увеличение активности проӯцессов гликоӯлиза при снижении активности беӯта-окисления жирных кислот посредством пряӯмого воздействия на транспортные системы пеӯреноса глюкозы в клетку;
- усиление активносӯти окислительного фосфорилирования и синтеза АТФ в митохондриях сопровождается повышеӯнием активности креатинфосфокиназной систеӯмы, что сопряжено с нормализацией окислиӯтельно-восстановительных процессор нарушаӯемых при дисциркуляторной энцефалопатии;
- усиление окисления NAD·H и генерации NAD+;
- усиление метаболизма накапливающегося при нарушении мозгового кровотока лактата, который используется для синтеза глюкозы и гликогена и способствует ускорению метаболизӯма пирувата путем присоединения низкомолекулярных радикалов в оксалоацетат с дальӯнейшим включением последнего в цикл Кребса.
- создаӯние физиологических концентраций глутамата, близких к верхней границе нормы, может опреӯделять ингибирование синтеза N0` в связи с блоӯкадой индуцибельной синтазы N0;
- восстановӯление уровня глутатиона в результате блокады S – нитрозиӯлирования и уменьшение активности пентозофосфатного пути.
Механизмы реализации психокоррегирующего эффекта Реамберина, лежащего в основе улучшения КЖ, могут быть связаны с основныӯми путями синтеза ГАМК с учетом эффекта Бэлша (компартментализация метаболизма глутамата, глутамина и ГАМК). Возможна активаӯция γ-глутамильного цикла. Представляется возможным влияние Реамберина на активность окислительного декарбоксилирования α-кетоглутарата с образованием сукцинил-КоА, так как данная реакция обеспечивает поддеӯржание суммарной концентрации метаболитов цикла на стационарном уровне. Образование α-кетоглутарата способствует его дальнейшему участию как в ЦТК, так и в глутаматӯдегидроӯгеназной и трансаминазной реакциях. Сукцинатдегидрогеназная реакция играет большую роль в энергетическом метаболизме при хрониӯческой гипоксии и обеспечивает поддержание энергетического баланса ткани, особенно на пи-ридиннуклеотидном участке дыхательной цеӯпи. Основными энергозависимыми процессами, функция которых улучшается при приеме Реӯамберина, являются: проведение нервных имӯпульсов; поддержание пространственной ориӯентации и конформации структурных единиц нейрона; образование синаптических структур, функционирование синапсов; нейрологическая память; трансмембранӯный перенос субстратов, нейромедиаторов; аксональный и ретроградӯный ток.
Выводы
Продемонстрирована необходимость разраӯботки «стратегии» оптимиӯзации режимов метаӯболической биорегуляции на примере одной ноӯзологии (СД тип 1) на основе комплексной сисӯтемы анализа фармакодчнамических эффектов инфузионного раствора «Реамберин 1,5%» Разработана новая платформа для фармакоки-нетического анализа при применении Реамбеӯрина 1,5% для инфузий.
Список литературы
- Дедов И.И., Сунцов Ю.И., Кудрякова С.В., Рыжкова С.Г. Эпидеӯмиоӯлогия инсулинзависимого сахарного диабета // Кардиология.- 1998.-№3.-C- 47-55.
- Claasification and Diagnosis of Diabetes Mellitus and Other Categories of Glucose Intolerance //Diabetes,- 1979,-Vol. 28,- P, 1039- 1057.
- Hoffman G.F. Organic acid analysis // Blau N., Du ran M., Blaskovics M.E., eds. Phisician`s guide to the laboratory diagnosis of metabolic diseases,- Chapman & Hall London, 1996,- P. 31-40.
- Holleland G.,. Schneede J,. Ueland P.M., Lund P.K., Ref'sum H., Sandberg S. Cobalamin deficiency in general practice. Assessment of the diagnostic utility and cost-benefit analysis of methylmalonic acid determination in relation to current diagnostic strategies//Clin.Chem,- 1999,- Vol. 45.- P.189-198.
- Pfeiffer С.М., Smith S.J., Miller D.T., Gunter E.W., Comparison of serum and plasma methylmalonic acid measurements in 13 laboratories: an international study // Clin.Chem. - 1999,- Vol. 45. – P2236-2242.