Ишемические поражения мозга преобладают среди цереброваскулярной
патологии [2]. Имеется множество эффективных, но дорогостоящих
нейропротекторов с метаболическим и вазорегулирующим действием [5,
9]. Однако, ограниченные ресурсы здравоохранения и, часто,
финансовая несостоятельность пациентов затрудняют их широкое
применение. Фармакоэкономический анализ типичной практики ведения
больных с ишемическим инсультом свидетельствует о высоких затратах
курсового лечения [3]. Это связано с количеством дней проведенных
в отделении интенсивной терапии и реанимации (ОИТиР), осложнениями
из-за госпитального истощения, длительностью пребывания в
стационаре, применением дорогостоящих современных препаратов
[2-5,12]. Высокая частота постинсультной инвалидизации и ее
неблагоприятные социально-экономические последствия для пациента,
его близких и общества диктуют необходимость новых медикаментозных
противоинсультных схем не только более эффективных клинически, но и
доступных экономически.
Повреждение мозга при ишемии обусловлено каскадом
патобиохимических перестроек в условиях экстремальных
энергозапросов ткани из-за гипоксии [2, 5, 9, 12, 14].
Энергопродукция, зависимая от обмена янтарной кислоты, играет
ключевую роль в сохранении метаболического гомеостаз нервной ткани,
как на разных этапах адаптации к ишемии, так и при
фармакологической коррекции гипоксии [14]. Несостоятельность
сукцинатзависимой биоэнергетики вследствие торможения
сукцинатдегидрогеназы (СДГ), напротив, приводит к каскаду
необратимых повреждений нервных клеток [14]. Согласно
доклиническим данным развитие патологии можно сдержать с помощью
интенсивного введения экзогенной янтарной кислоты (в виде солей)
[7]. Средством, обладающим универсальным полиорганным
энергопротекторным действием является реамберин (Р) –
плазмозаменитель на основе янтарной кислоты [1,11]. Опубликованные
сведения о фармакодинамике этого препарата [1], наши собственные
наблюдения [13], а также данные о фармакоэкономических эффектах
других средств, содержащих митохондриальные субстраты [8],
позволяют предположить, что введение Р в схему лечения пациентов в
острый период ишемии мозга не только усилит клинический эффект
[11], но и снизит затраты на лечение.
Для объективной оценки действия реамберина по всей совокупности
неоднородных признаков необходим системный анализ сложных
взаимодействий входных факторов и разнородных
параметров-откликов.
Цель работы состояла в изучении эффективности Р при
ишемическом инсульте с использованием многомерного факторного
анализа клинических и фармакоэкономических показателей и условиях
неоднородности и многообразия клинических данных.
Материалы и методы. В ходе ретроспективного
клинико-экономического исследования по методу «анализ стоимости
болезни» и «анализ затраты-эффективность» [3, 10] сопоставляли две
схемы ведения пациентов с диагнозом «ишемический инсульт»
подтвержденным клинически и нейровизуализационно, впоследствии
выписанных из стационара. Больные поступали в отделение интенсивной
терапии и реанимации (ОИТиР) в первые 48 часов от начала
заболевания. Случайным образом формировали группу из 76 пациентов.
43 получали препараты типичной практики (ПТП), а 33 пациентам к
препаратам типичной практики в ОИТиР добавляли Р (ПТП+Р). При
поступлении группы были симметричны по тяжести состояния и основным
неврологическим симптомам (табл. 1). Эффективность лечения
оценивали по совокупности параметров-откликов, фиксированных в
историях болезни и отражающих динамику состояния пациентов при
поступлении в стационар и при выписке.
Прямые медицинские затраты на ведение пациентов в стационаре
рассчитывали, включая стоимость койко-дня в ОИТиР, в
неврологическом отделении (по данным экономического отдела
больницы), затраты на лекарства.
Цены на лекарственные средства были взяты из прайс-листа
регионального дистрибъютоpa медицинских препаратов «Протек». Все
экономические данные соответствовали периоду наблюдений 2004-2005
гг. При статистической обработке результатов матрицу исходных
данных размерностью 152*43 поэтапно анализировали в
модуляхANOVA/MANOVA, Nonparametric statistics, Principal components
&Classification Analysis ППП STATISTICА 6,0.
В качестве группирующих факторов выделяли признаки «тип
фармакотерапии» (ПТП и ПТП+Р) и «период наблюдения (до лечения,
при выписке). Редукцию многомерной информации проводили методом
главных компонент (ГК) до первых двух факторов F1 и
F2 поглощающих максимум дисперсии исходного массива
данных [6].
Результаты и их обсуждение. Клиническая результативность
двух медикаментозных схем при попарном сопоставлении групп при
выписке оказалась практически одинаковой (табл. 2). Артериальное
давление (основной фактор риска острой недостаточности мозгового
кровообращения) у большинства пациентов при выписке
нормализовалось, как по средним величинам, так и по частоте
встречаемости его оптимальных значений.
Лейкоцитарный индекс интоксикации (ЛИИ) также указывал на
состояние либо «легкой тяжести», либо «нормы» практически у всех
пациентов. Однако, данные общего анализа крови показали, что в
группе ПТП+Р выраженность воспалительных процессов была несколько
ниже, чем в контрольной.
Неврологическая симптоматика при выписке также указывала на
наличие тенденции более существенного клинического эффекта у
пациентов ПТП+Р. В этой группе доля пациентов, выписанных с
остаточными нарушениями речи и двигательной активности, были на 11
и 14% ниже, чем при традиционном лечении. Применение Р
препятствовало нарушениям функции печени (активность АЛТ и ACT за
период лечения изменялась минимально) и повреждению гепатоцитов
(коэффициент Де Ритиса) из-за ксенобиотической нагрузки лекарствами
в критический период при лечении в ОИТиР. В отличие от группы ПТР+Р
в группе ПТП 16% пациентов повторно направлялись в ОИТиР с
осложнениями. Как показал дальнейший анализ, Р способствовал
повышению клинической эффективности лечения на фоне более коротких
сроков пребывания в стационаре (табл. 3).
Таблица 1. Характеристика пациентов» включенных в исследование,
при поступлении в клинику
|
Показатель
|
Группа сравнения
|
|
ПТП (n=43)
|
ПТП+Р (n=33)
|
|
Возраст, лет (М ± m)
|
65 ± 4
|
64 ± 4
|
|
Распределение по полу (М/Ж)
|
21/22
|
17/14
|
|
САД, мм. рт. ст. (М ± m)
|
156 ± 14
|
152±13
|
|
ДАД, мм. рт. ст. (М ± m)
|
95±8
|
91±6
|
|
ЧСС, уд/мин (М ± m)
|
85±6
|
88 ± 6
|
|
Доля пациентов с САД < 140 мм рт. ст., %
|
29
|
26
|
|
Доля пациентов с ДЛД < 90 мм рт. ст., %
|
35
|
42
|
|
Снижение уровня сознания, % пациентов в группе
|
65
|
55
|
|
Менингиальные знаки, % пациентов в группе
|
3
|
3
|
|
Нарушения речи, % пациентов в группе
|
71
|
68
|
|
Двигательные расстройства,
% пациентов в группе
|
90
|
81
|
|
Нарушения чувствительности,
% пациентов в группе
|
0
|
10
|
|
Уменьшение мышечного тонуса,
% пациентов в группе
|
3
|
13
|
|
Нарушение глотания, % пациентов в группе
|
13
|
16
|
|
Нарушения функции черепно-мозговых нервов,
% пациентов в группе
|
32
|
35
|
|
Нарушения функций тазовых органов,
% пациентов в группе
|
0
|
3
|
|
Лейкоцитарный индекс интоксикации
по Кальф-Калифу, баллы (М ± m)
|
3,8 ± 1,5
|
4,4 ± l,4
|
|
ЛИИ < 1,5, % пациентов в группе
|
38
|
19
|
|
Гематологический показатель интоксикации,
баллы (М ± m)
|
43± 17
|
35 ± 11
|
|
АЛТ(М ± m)
|
29± 3
|
36± 5
|
|
ACT (М ± m)
|
37± 4
|
44± 5
|
|
Коэффициент Дс Ритиса (М ± m)
|
1,37 ±0,1
|
1,35 ± 0,1
|
Таблица 2. Клинические параметры разных схем фармакотерапии
ишемического инсульта при выписке
|
Параметр клинической эффективности
|
Группы сравнения
|
р
|
|
ПТП
|
ПТП+Р
|
|
САД, мм. рт. ст (М ± m)
|
125 ± 6
|
124 ±5
|
нд
|
|
ДАЦ, мм. рт. ст (М ± m)
|
79 ± 3
|
79 ±3
|
нд
|
|
ЧСС, уд/мин (М ± m)
|
77 ±4
|
76 ±4
|
нд
|
|
Доля пациентов с САД < 140 мм рт. ст.,%
|
74
|
74
|
нд
|
|
Доля пациентов с ДАД < 90 мм рт. ст.,%
|
87
|
91
|
нд
|
|
Средние значения ЛИИ по группе (М ± m)
|
1,2 ±0,1
|
2,1 ±0.5
|
0,021
|
|
Доля пациентов в группе с ЛИИ < 1,5, %
|
77
|
71
|
нд
|
|
АЛТ (М ± m)
|
34*4
|
36 ±3
|
нд
|
|
АСТ(М ± m)
|
48=: 7
|
41±4
|
0,04
|
|
Коэффициент Дс Ритиса (М ± m)
|
1,7 ±0,2
|
1,1 ±0,05
|
0,045
|
|
Доля пациентов
с нормализацией коэффициента Де Ритиса, %
|
39
|
71
|
0,02
|
|
Доля пациентов
с остаточными нарушениями речи, %
|
01
|
50
|
0,07
|
|
Доля пациентов
с остаточными двигательными нарушениями, %
|
84
|
70
|
нд
|
|
Доля пациентов
с повторными поступлениями в ОИТиР, %
|
16
|
0
|
-
|
*Примечание:
р – уровень статистической значимости межгрупповых различий по
критериям Монна-Уитни, t-Стьюдента, Хи-квадрат, в зависимости от
типа распределения.
НД – различия статистически недостоверны.
Пациенты, получавшие дополнительно Р, переводились из ОИТиР в
среднем на 24 часа раньше (диапазон максимального времени
пребывания у группы ПТП+Р почти в три раза короче). Время
пребывания в неврологическом отделении и общая длительность
госпитализации у пациентов этой группы также сокращались в среднем
на 5 суток, а минимальные, максимальные и наиболее часто
встречающиеся сроки госпитализации указывали на еще более
существенные различия (до 10 суток).
Согласно фармакоэкономическому анализу при использовании Р
затраты на лечение также существенно уменьшались (табл. 3).
Таблица 3. Структура прямых затрат при лечении ишемического инсульта
в группах сравнения
|
Показатели
|
Группы сравнения
|
Р
|
|
ПТП
|
ПТП+Р
|
|
Сроки пребывания в разных отделениях стационара и
их стоимость
на курс лечения 1 пациента
|
|
В ОИТиР, дней, (М ± m)
[min; max]. Mo
|
5,6 ± 1,6
[1;25]. 3
|
4,8 ± 0,8
[2; 9]. 2
|
Нд
|
|
В неврологическом отделении, дней, (М ± m)
[min; max]. Mo
|
22.5 ±3
[11; 52]. 23
|
17,7±2,5
[7; 36]. 12
|
0,004
|
|
Общая длительность лечения,
(М ± m)
[min; max]. Mo
|
26,8 ±3
[14; 57]. 28
|
22,5±2,9
[9; 41]. 18
|
0,025
|
|
Затраты в ОИТиР, рублей, (М ± m)
[min; max]. Mo
|
16333±3426
[3308;39696]. 9924
|
15900±2792
[6616;29772]. 6166
|
Нд
|
|
Затраты в отд. неврологии, рублей, (М ± m)
[min; max]. Mo
|
21263 ±2550
[10395; 49140]. 21735
|
16766 ±2396
[6615;34020]. 11340
|
0,004
|
|
Общие затраты (включая лекарства), рублей, (М ± m)
[min; max]. Mo
|
40363 ±5399
[21608; 77972]. 35648
|
35426 ±4540
[15484;57168]. 32761
|
0,004
|
|
Стоимость медикаментов, в рублях на курс лечения
1 пациента
|
|
Антибиотики, (М ± m)
[min; max]. Mo
|
529
[30; 3440], 138
|
514
(48; 1502], 69
|
Нд
|
|
Гипотензивные, (М ± m)
[min; max]. Mo
|
143
[2; 496], 123
|
51
[3:228], 38
|
0,005
|
|
Антикоагулянты, (М ± m)
[min; max]. Mo
|
813
[39:228], 159
|
76
[1;183], 50
|
0,001
|
|
Инфузионно-трансфузионные средства, (М ± m)
[min; max]. Mo
|
1109
[50; 7102]. 366
|
1455
[338;3699], 482
|
0,005
|
|
Нейропротекторы, (М ± m)
[min; max]. Mo
|
866
[30:3841]. 61
|
699
[3;2176], 45
|
Нд
|
|
Другие препараты, (M ± m)
[min; max]. Mo
|
94
[l;90], 12
|
17
[3;414]. 6
|
0,02
|
|
Общая стоимость лекарств, (М ± m)
[min; max]. Mo
|
3054
[324; 122921]
|
2738
[728; 7161]
|
0,07
|
*Примечание:
Значение некоторых параметров не подчинялись нормальному
распределению, поэтому для более четкого выявления деталей
межгрупповых различий приведены не только средние величины (М) с
ошибкой средней (m), но и минимальные (min), максимальные (mах) и
наиболее часто встречающиеся значения параметров (Мо). Курсовая
доза Р в группе ПТП+Р (в виде внутривенных инфузий по 400 мл/сут)
составила 2200±560мл (min – 800; max – 6400) Мо 1200мл. В группе
ПТП+Р дополнительные затраты на введение Р в среднем составили на
курс лечения 1 пациента 831±179 рублей, (min – 288; max – 2304) Мо
– 432 рубля.
Усредненная стоимость пребывания пациентов обеих групп в ОИТиР
оказалась почти одинаковой, однако наиболее часто встречающиеся
затраты и максимум их значений различались в пользу группы ПТП+P на
3308 и 9924 рубля за курс лечения, соответственно. Согласно анализу
стоимости болезни по методу минимизации затрат [3,10] использование
Р в схемах традиционного медикаментозного ведения пациентов с
ишемическим инсультом снижало общую стоимость лечения. Структура
затрат на лекарственные средства для достижения необходимого
клинического эффекта на фоне Р изменялась: максимальные затраты на
антибиотики по группе ПТП+Р и типичная их стоимость оказались ниже.
Затраты на гипотензивные средства, антикоагулянты и средства
инфузионно-трансфузионного сопровождения в этой группе также
уменьшались. По средней стоимости нейропротекторов группы
статистически не различались, но основные характеристики ряда
данных свидетельствовали об уменьшении затрат и на этот тип
препаратов у большинства пациентов группы ПТП+Р. Таким образом,
введение Р в схему типичной медикаментозной практики при
ишемическом инсульте обеспечивало высокую клиническую
эффективность вмешательства с сокращением сроков выхода из
критического состояния и постишемической реабилитации в
стационаре, снижение ксенобиотической нагрузки на печень,
уменьшением расходов на медикаменты и общую медицинскую услугу.
Фармакоэкономический анализ, проведенный по методу «стоимость –
эффективность» [3, 11], показал, что коэффициент CER
(costeffectiveness ratio), рассчитанный как величина затрат в
рублях на единицу эффекта в группе ПТП+Р снижен примерно вдвое
(табл. 4). Следовательно, взаимодействие факторов, обеспечивших
повышение клинико-экономической эффективности Р обусловило снижение
затрат на достижение единицы клинического эффекта. У пациентов в
критическом постинсультном состоянии, сопровождающемся мощной
дизрегуляцией, гипоксией и энергодефицитом, реализовалось
полиорганное энергопротекторное действие Р.
Его благотворные эффекты проявились на разных уровнях
биологической интеграции и обеспечили ускорение выздоровления и
фармакоэкономическую эффективность. В ходе факторного анализа это
многокомпонентное сложное явление формально представили как триаду
«больной организм – базисные средства лечения – реамберин и в
обобщенном виде оценили эффективность Р с позиций многомерности,
учитывающей сложность взаимодействий входных факторов и
неоднородность параметров – откликов.
Факторный анализ разнородных и разнонаправлен пых
параметров-откликов позволил выявить связи между ними и
группирующими признаками «период наблюдения» и «тип фармакотерапии»
(рис. 1). ГК F1 и F2 поглощали 58% дисперсии
массива. По факторным нагрузкам F1 (47% дисперсии
массива) ассоциировалась с «периодом наблюдений». Ее
интерпретировали как вектор саногенеза.
Таблица 4. Фармакоэкономические показатели эффективности
введения реамберина в схему фармакотерапии ишемического
инсульта (на курс лечения 1 больного)
|
Условные единицы клинической эффективности вмешательства
|
Значения CER
(рубли на единицу эффективности)
|
Вектор CER, %
|
|
ПТП
|
PTP+P
|
|
Улучшение состояния 1% пациентов
по критерию ЛИИ < 1,5
|
1302
|
С95
|
-46
|
|
Устранение нарушений речи
у 1% пациентов
|
4036
|
1968
|
-51
|
|
Устранение двигательных нарушений
у 1% пациентов
|
6727
|
3220
|
-52
|
|
Затраты на гипотензивные средства
для снижения САД на 10 мм рт. ст.
|
46
|
19
|
-58
|
|
Затраты на гипотензивные средства
для снижения ДАД на 10 мм рт. ст.
|
89
|
42
|
-58
|
|
Затраты на нормализацию коэффициента Де Ритиса у 1%
пациентов
|
1035
|
499
|
-52
|
F2 (11% дисперсии массива) ассоциировалась с «типом
фармакотерапии» и играла вспомогательную роль. Показатели-отклики
оказывали разные факторные нагрузки на F1 и
F2 Поэтому все пациенты (они формально представлены
точками с координатами по осям F1 и F2) были
«организованы» в виде компактных сообществ, характеризующие группы
сравнения до лечения и при выписке. Согласно вектору саногенеза (по
F1) основное сгущение точек, характеризующих пациентов
до лечения, находилось в отрицательной области или возле нуля. При
выписке большинство точек перемещалось в область положительных
значений, причем общность ПТП+Р оказалась более продвинутой вправо
по F1 чем группа ПТП, что свидетельствовало о более
высокой эффективности лечения и ускорении выздоровления. Таким
образом, при многомерном представлении пациентов по совокупности
клинических параметров, группы сравнения дифференцировались по типу
фармакотерапии и ее эффективности.
Многомерная оценка фармакоэкономической эффективности
вмешательства по совокупности всех показателей подтвердила
лидирующее положение группы, получавшей Р (рис. 2). Массив
фармакоэкономических данных редуцировали до F1 и
F2, поглотивших 74% дисперсии. Факторные нагрузки
экономических показателей на F1 (46% дисперсии)
преобладали. Ее интерпретировали как вектор «фармакоэкономического
преимущества» (рис. 2. А)
Формальное представление пациентов при выписке в координатах
F1 и F2, характеризующих затраты на лечение,
свидетельствовало об экономии ресурсов в группе получавшей Р (рис.
2. Б). Точки группы ПТП собирались в обширное сгущение,
превосходящее по площади группу ПТП+Р, которая была смещена правее
по F1 что свидетельствовало об экономическом эффекте
Р.
Схемы назначений и анализа в группах пациентов с ишемическим
инсультом были симметричными, отличия касались лишь применения Р.
Следовательно, межгрупповые различия клинической и
фармакоэкономической эффективности результатов лечения
обусловлены именно многогранным воздействием этого инфузионного
энергопротектора. Системный подход как методологический анализ
многомерного уровня, позволил учесть неоднородность информации,
многообразие связей между клиническими, фармакологическими и
экономическими элементами формализованной триады «пациент –
базисная терапия – энергопротектор» и сравнить группы пациентов в
зависимости от этапа лечения, типа и эффективности фармакотерапии.
Группам пациентов с ишемическим инсультом практически одинаковым по
тяжести состояния при поступлении в стационар, была оказана
клинически эффективная медицинская неврологическая помощью. На фоне
дополнительного применения Р неврологическая динамика была более
благоприятной, повреждения детоксицирующей системы печени
минимизированы, а сроки выздоровления – существенно снижены.
Ведущий фармакодинамический компонент препарата Р – янтарная
кислота, обладающая полиорганным энергопротекторным действием,
способствовала мобилизации адаптивных ресурсов организма при
восстановлении в постинсультный период и обеспечивала
фармакодинамическое потенцирующее взаимодействие базисных средств,
а также существенное снижение стоимости лечения.
Вывод, Схема фармакотерапии ишемического инсульта с применением
реамберина обладает более высокой клинической и экономической
эффективностью, что позволяет отнести ее к доминирующей
клинико-экономической альтернативе.
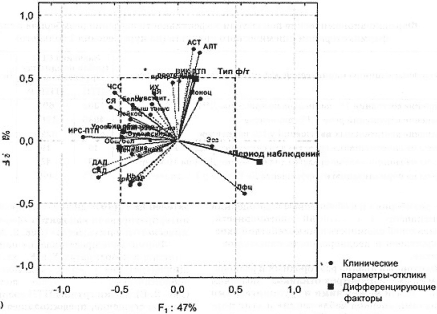
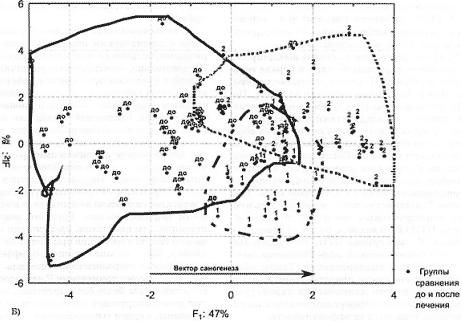
Рис. 1. Эффективность реамберина в схеме комплексной
фармакотерапии пациентов с ишемическим инсультом
Пояснения к рис. 1:
А – Факторные нагрузки на F1 и F2 множественных корреляции
параметро-откликов, характеризующих клиническую эффективность
лечения, их информативность в отношении дифференцировки групп
сравнения. К значимым отнесены маркерные показатели, у которых
факторные нагрузки на F1 и F2 превышают 0,5 (пограничная область
обозначена пунктиром).
Б – представление пациентов до и после лечения в пространстве
многомерных факторов клинической эффективности типа
фармакотерапии. 1 группа – ПТП; 2 – группа ПТП±Р. По F1 – стрелкой
указан вектор саногенеза (клинического преимущества).
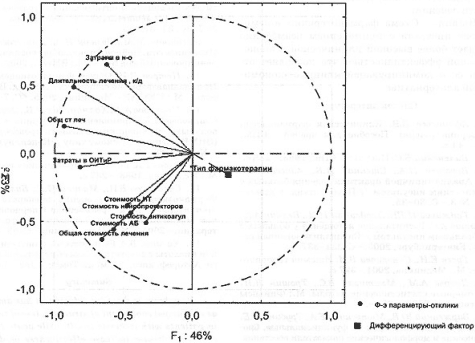
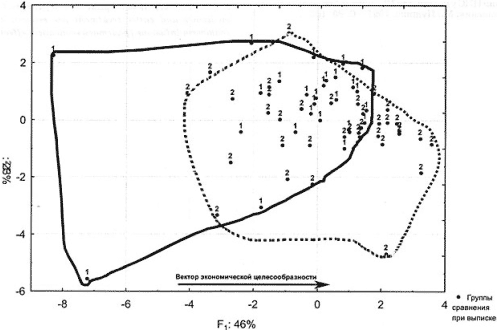
Рис. 2. Экономическая целесообразность применения
реамберина
при лечении ишемического инсульта
Пояснения к рис. 2:
А – информативность экономических параметров-откликов, согласно
их факторным нагрузкам на ГК.
Б – фармакоэкономические характеристики пациентов после разных
схем вмешательства при выписке. 1-группа ПТП; 2 – группа ПТП+Р.
Стрелкой обозначен вектор «экономического преимущества».
Список литературы:
- Афанасьев В.В. Клиническая фармакология реамберина
(очерк): Пособие для врачей. СПб., 2005.- 44 с.
- Виленский Б.С. Инсульта СПб., 1995. – 288 с.
- Воробьев И. А., Степная И. Ж., Авксентьева М.В.
Анализ типичной практики ведения больных с ишемическим инсультом //
Пробл. станд. в здравоохр.- № 3.- С. 30-35.
- Гаджиева Н.Ш., Лепдерман И.Н., Белкин А.А.,
Солдатов А.С. Госпитальное истощение у больных с церебральным
инсультом//Специализированная помощь. Екатеринбург 2005.- С.
334-337.
- Гусев Е.И., Скворцова В.М., Ишемия головного мозга.
M. Медицина, 2001.-327 с.
- Дубров А.М. Мхитарян B.C., Трошин Л.И. Многомерные
статистические методы. М.: Финансы и статистика 2000.- 352 с.
- Заржецкий Ю.В., Мутускина Е.А., Трубина И.Е.
Влияние сукцината натрия на функциональные, биохимические и
морфологические показатели восстановления ЦНС у крыс после
10-минутной остановки кровообращения. М.: Пущино, 1997.-С.
96-103.
- Мазина Н.К., Хазанов В. А. Регуляторы
энергетического обмена и оптимизация затрат на медикаментозные
вмешательства // Фарматека. 2004.-№7.- С. 34-87.
- Одинак М.М., Вознюк И.А., Янишевский С.И. Ишемия
мозга. Нейропротективная терапия. Дифференцированный подход. СПб.:
ВмедА, 2002.- 77 с.
- Петров В.И. Общая фармакоэкономика. // Прикладная
фармакоэкономика / Под ред. В.И. Петрова. - М.: ГЭОТАР - Медицина,
2005.- С. 7-25.
- Привалов А.А., Холманских Н.В., Обухов Н.Г.,
Свиридова Л.К. Применение реамберина в лечении больных с
нарушениями мозгового кровообращения (ОНМК) по ишемическому типу
//Консилиум. - 2005 -№ 4.-С. 28-29.
- Рябов Г.А. Гипоксия критических состояний. М.:
Медицина, 1088.- 287 с.
- Сухоруков В.П., Мазина Н.Ж. Булдаков А.В.
Фармакоэкономическая оценка препарата энергопротекторного типа –
реамберина в периоперационном обеспечении резекций печени //Вестн.
интенс. терапии.- 2005.- № 5, Приложение. - С. 68-69,.
- Хазанов В.А. Роль системы окисления янтарной
кислоты в энергетическом обмене головного мозга: Автореф. дис…
д.м.н., Томск, 1993.- 84 с.