В последнее время прослеживается тенденция к созданию ноотропов
не только на основе оригинальной химической субстанции, но и в
результате комбинирования ноотропа с препаратами, усиливающими
его позитивные свойства. Подобным комбинированным ноотропным
препаратом, является Тиоцетам, разработанный АО «Галычфарм»
совместно с НВТ «Фарматрон» [49, 50, 51].
Этот оригинальный комбинированный препарат, содержащий в составе
базовый рацетам – пирацетам и антиоксидант – тиотриазолин.
Обоснованием для его применения с целью профилактики и коррекции
когнитивных дисфункций явилось удачное сочетание целенаправленного
воздействия препарата одновременно на многие звенья
метаболизма.
Пирацетам проявляет свойства психостимулятора с особым акцентом
действия на интеллектуальную сферу больных и обладает
антидепрессивной активностью, уменьшает экстрапирамидные
дисфункции, повышая корковый контроль над подкорковыми
образованиями у больных инсультом. Препарат повышает интенсивность
альфа-ритма в пораженном полушарии и снижает интенсивность
тета-ритма в здоровом. Улучшает восприятие, особенно зрительное,
способность концентрировать внимание, стимулирует речевую функцию
[45, 49, 52, 53].
Эффекты тиоцетама
Основными эффектами тиотриазолина являются: кардиопротекторный,
антиаритмический, гепатопротекторный, церебропротекторный,
антиоксидантный, противоишемический,
противовоспалительный, иммуномодулирующий. В основе
противоишемического действия тиотриазолина лежит его способность
снижать степень угнетения окислительных процессов в цикле Кребса с
сохранением внутриклеточного фонда АТФ, стабилизировать
метаболизм кардиомицитов.
Тиотриазолин активирует антиоксидантную систему ферментов и
тормозит процессы перекисного окисления липидов в ишемизированных
участках миокарда. Активирует антирадикальные ферменты –
супероксиддисмутазу и каталазу, антиперекисные ферменты –
супероксиддисмутазу, способствует более экономному расходу
эндогенного антиоксиданта – токоферола.
Противовоспалительное действие обусловлено уменьшением явлений
отека в измененных тканях и улучшением процессов микроциркуляции за
счет снижения вязкости крови. Тиотриазолин обладает высокими
гепатопротекторными свойствами. При всех видах патологии печени
показана его высокая антиоксидантная активность. Он быстро
устраняет из крови и тканей продукты свободнорадикального окисления
– главный повреждающий фактор гепатоцитов, устраняет
диспротеинемию, повышает уровень общего белка и альбуминов.
Тиотриазолин улучшает дезинтоксикационную функцию печени, о чем
свидетельствует нормализация уровня белков, мочевины и глюкозы в
крови. Иммуномодулирующее действие выражается в снижении или
нормализации количества больших, средних и малых циркулирующих
иммунных комплексов.
Тиотриазолин обладает высоким церебропротекторным действием. В
острой фазе ОНМК приводит к существенному снижению биохимического
маркера повреждения мозговой ткани – активности ВВ-КФК, снижает
интенсивность анаэробного гликолиза (снижение лактата), активирует
реакции цикла трикарбоновых кислот (увеличивает содержание малата).
Повышает уровень макроэргов в острый период ОНМК. Антиоксидантный
эффект заключается в снижении уровня накопления продуктов
свободнорадикального окисления в ткани мозга – диеновых конъюгатов
и малонового диальдегида, увеличивается активность
супероксиддисмутазы, каталазы, глутатионпероксидазы, содержание
α-токоферола.
Противоотечное действие состоит в снижении явлений
периваскулярного, перицеллюлярного и апикально-дендритного отеков,
уменьшении числа ишемически изменненых нейронов и спавшихся
капилляров, что является ведущим патогенетическим фактором гибели
нейронов в острый период ОНМК.
За счет тиотриазолина тиоцетаму характерен более широкий спектр
ноотропного действия, чем для пирацетама отдельно, так как он
действует только на начальных этапах формирования памяти, а
тиоцетам положительно влияет на процессы первичной обработки
информации, ее фиксацию и консолидацию. Значительно активирует
пролиферацию клеток глии и их функцию, вызывает усиление
сателлитолиза, что является ведущим фактором обеспечения
жизнедеятельности нейронов при развитии ишемических повреждений
головного мозга. Тормозит истощение запасов глюкозы и гликогена в
нейронах в острый период ОНМК и внутримозгового кровоизлияния.
Показатели окислительной продукции энергии (НАД/НАДН, цитохром
С-оксидаза, уровень пирувата, малата и изоцитрата) становятся выше.
Поддержание тиоцетамом углеводного метаболизма определяет
повышение уровня макроэргов (АТФ, креатинфосфат). Пирацетам в этих
условиях оказывает преимущественное влияние на анаэробные пути
образования энергии, а тиоцетам на восстановление аэробных путей
продукции энергии.
Тиоцетам, не оказывая влияния на снижение уровня белка в
цитоплазме и митохондриях ишемизированных нейронов, существенно
тормозит нарастание фонда свободных аминокислот и их
нейродеструктивное действие. Тиоцетам увеличивает уровень РНК в
тканях мозга у больных с ОНМК и внутримозговым кровоизлиянием,
что указывает на активацию процессов протеинсинтеза и является
адаптационной реакцией на гипоксию, обеспечивающей перестройку
метаболизма мозга без повышения потребности в кислороде. Сам по
себе пирацетам не оказывает выраженного влияния на процессы синтеза
РНК в тканях мозга. Проявляет антикоагулянтную и фибринолитическую
активность, усиливает дестабилизацию фибрина [38, 50, 51].
Технология применения тиоцетама
(декларационный патент №23959/2004).
Тиоцетам назначался нами по ступенчатой схеме:
- насыщающая доза – по 25 мл (содержит 2,5 г пирацетама и 0,625 г
тиотриазолина) внутривенно капельно, начиная с первых минут
послеоперационного периода;
- поддерживающая доза – по 25 мл внутривенно капельно на
протяжении 7 суток, затем по 2 таблетки (1 таблетка содержит 1,2 г
пирацетама и 0,3 г тиотриазолина) 3 раза в день в течение 21
дня.
Анализ результатов исследования когнитивных характеристик у
больных, в комплекс интенсивной терапии в послеоперационном периоде
которых был включен тиоцетам, показал, что, несмотря на самый
низкий исходный уровень когнитивных способностей у этих больных (в
дооперационном периоде ниже среднего) на 5-е сутки после операции
мы не наблюдали снижения когнитивного фона, как это имело место у
больных контрольной группы (рис. 14).
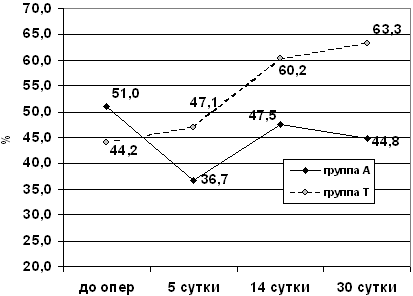
Рис. 14. Динамика когнитивных функцийу больных контрольной
группы и группы больных, получавших тиоцетам
Более того, показатель когнитивных характеристик возрастал до
среднего уровня по отношению к исходному результату этой группы
больных и превышал уровень когнитивного фона в других группах в
этот послеоперационный период (47,1±4,1%).
На 14 сутки после операции выявлено значительное, статистически
достоверное улучшение высших психических функций (р < 0,05).
Больные правильно решали в среднем 60,2±3,8% заданий, что
соответствует согласно критериальным оценкам когнитивных
характеристик уровню выше среднего. Такое повышение когнитивного
фона значительно опережает процессы соматического восстановления
больных, и достоверно значимо превышает результаты, полученные у
больных контрольной группы и группы, где использовался
реамберин.
Это свидетельствует о благотворном влиянии Тиоцетама на
психические процессы в раннем послеоперационном периоде. Применение
его позволяет не только сохранить исходное состояние когнитивных
функций у больных пожилого возраста, но и существенно его
улучшить.
На 30 сутки после операции наблюдалась дальнейшая положительная
динамика состояния высших психических процессов по сравнению с
предыдущим этапом. При этом когнитивные показатели оставались в
пределах оценок выше среднего уровня (63,3±3,2%).
При качественном анализе ошибок, допущенных больными группы с
использованием Тиоцетама при выполнении тестовых заданий в
отдаленном послеоперационном периоде (на 30-е сутки после
операции) установлено, что тенденция, наметившаяся в группе с
применением Реамберина, в этой группе получила более широкое
развитие: увеличивалась частота ошибок второго типа, связанных с
восприятием предметов и нахождением аналогии между парами фигур, с
динамической внимательностью при существенном уменьшении частоты
ошибок 4 и 5-го типов, что свидетельствует о значительном усилении
функции абстрактного и логического анализа после применения
Тиоцетама (рис.15).
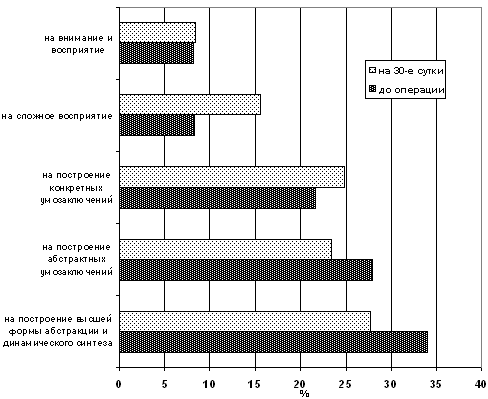
Рис. 15. Частота ошибок при выполнении тестовых заданий
больными группы Т в начале и в конце исследования
При использовании Тиоцетама побочных эффектов не наблюдалось.
Все больные препарат переносили хорошо.
Сравнительная оценка разных вариантов профилактики когнитивных
дисфункций в послеоперационном периоде представлена на рис. 16 и
17.
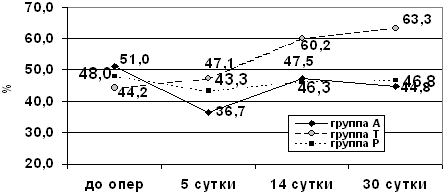
Рис. 16. Сравнение динамики когнитивных функций
у больных обследованных групп
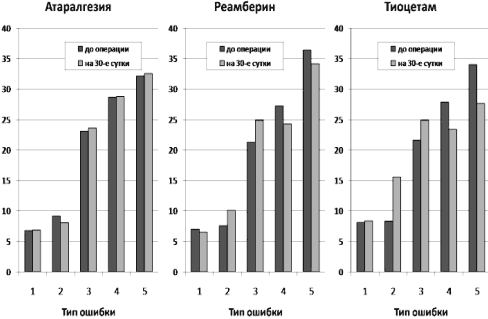
Рис. 17. Сравнение характера ошибок у обследованных
больных
при применении разных вариантов защиты когнитивных функций
Как видно, при применении Реамберина в послеоперационном периоде
удается сохранить количественно и качественно исходный уровень
высших психических функций.
Включение в комплекс интенсивной терапии в послеоперационном
периоде Тиоцетама позволяет не только сохранить когнитивные функции
в пределах исходных величин, но и достоверно их повысить с
улучшением более сложных психических функций, связанных со
способностью к аналитико-синтетической мыслительной
деятельности.
Вышеизложенное доказывает высокую эффективность Тиоцетама как
препарата, обладающего нейропротективным действием, способного
предотвратить нарушения когнитивных функций в послеоперационном
периоде у больных пожилого возраста, риск возникновения которых
связан с оперативным вмешательством и видом анестезии.
Он может быть рекомендован как препарат выбора в комплекс
интенсивной терапии в послеоперационном периоде для предупреждения
развития когнитивных дисфункций, как в раннем, так и в более
отдаленном послеоперационном периоде.
49. Беленичев И.Ф. Сидорова И.В. (2004) Тиоцетам - новый церебропротекторный и ноотропный препарат // Новости медицины и фармации. - 2004. - №13. - С.3-4.
50. Кузнецова С.М., Юрченко Ф.В. Влияние тиотриазолина на функциональное состояние ЦНС у больных, перенесших ишемический инсульт // Здоров'я України. - 2006. - №10. - С.46-49.
51. Середа Д.А. Дейниченко Ю.К., Беленичев И.Ф., Мазур И.А, Бурлай В.З. Терапевтическая эффективность нового церебропротективного и ноотропного препарата тиоцетам в остром периоде тяжелой ЧМТ // Медицина неотложных состояний. - 2006. - №2(3). - С.15-17.
52. Старченко А.А. Клиническая нейрореаниматология. СПб.: Санкт-Петербургское медицинское издательство. - 2002. - 672 с.
53. Стец В.Р., Беленичев И.Ф., Мазур И. А., Сидорова И.В. Ноотропная терапия: прошлое, настоящее и будущее. Здоров'я України. - 2004. - №18. - С.1-3.