Источник: Вопросы онкологии. 2012. №1. С.110-114
Статья процитирована в PubMed. PMID: 22629839
ГМУ «Новгородский областной клинический онкологический диспансер», Великий Новгород
Применение реамберина
для снижения опухолевой интоксикации и побочных действий
в комбинированном лечении рака яичников III-IY стадий
В.Г. Черенков, А.Б. Петров, А.А. Шпенкова, Т.М. Васильева
Черенков Вячеслав Григорьевич, д.м.н.,проф. – Великий Новгород, 173016. ул.Ломоносова, 27. Областной клинический онкологический диспансер, руководитель отдела инноваций, научной и консультативной работы
Петров Александр Борисович, канд.мед.наук – Великий Новгород, 173016. ул.Ломоносова, 27. Областной клинический онкологический диспансер, главный врач
Шпенкова Алла Анатольевна, канд мед.наук, зав. онкогинекологическим отделением НОКОД
Васильева Татьяна Михайловна, врач-химиотерапевт
Лечение рака яичников ввиду высокой частоты запущенных случаев
(III-IY стадий), тяжелых осложнений, связанных с асцитом и
интоксикацией является во многих аспектах не решенной проблемой. В
работе показаны возможности применения отечественного препарата
реамберин для снижения интоксикации и побочных действий, которые
являются основным объектом, препятствующим эффективному применению
специальной терапии. Изучены результаты применения реамберина у 89
больных асцитным раком яичников III-IY стадий по классификации FIGO
в возрасте от 42 до 79 лет после циторедуктивной операции и в
процессе жестких курсов полихимиотерапии (по схеме СР и САР) для
снижения побочных действии. Установлено, что в исследуемой группе
гематологические показатели (анемия и лейкопения 1-2 степени) и
частота нарушений функций сердечной деятельности были значительно
ниже, чем в контрольной группе. Разница статистически достоверна
(соответственно p< 0,01 и p< 0,05). В группе больных,
получавших реамберин в качестве предхимиотерапевтической
подготовки и в процессе ПХТ лишь в 3,37% больных сохранилось
повышение уровня креатинина, тогда как в контрольной группе число
больных с уровнем креатинина (1-3 степени) увеличилось у 41,4%, что
потребовала в 12 случаях (14,6%) приостановления химиотерапии,
проведения коррегирующей терапии. Разница между группами
статистически достоверна (p< 0,001). Снижение опухолевого
маркера СА-125 констатировано в более короткие сроки, чем в
контрольной группе. Дисперсионный анализ (F-тест) показал, что
эффекты различий снижения Са –125 после 2, 4 и 6 курса, значимые
на уровне р<0,05. Таким образом, реамберин
является универсальным препаратом для снижения интоксикации и
протектором побочных действий специальной терапии рака яичников без
ослабления противоопухолевого эффекта.
Введение
В большинстве стран мира рак яичников имеет самые высокие
показатели смертности среди всех гинекологических опухолей, что
связано с поздней диагностикой заболевания. Летальность больных
раком яичников в течение первого года после взятия на учет
превышает 35%. По сводным данным раковых регистров стран Европы
одногодичная выживаемость больных раком яичников составляет 63%,
3-х летняя выживаемость – 41%, 5-летняя – 35%. За десятилетие
платиновая химиотерапия в лечении распространенных форм рака
яичников позволила повысить 5-летнюю выживаемость после оптимальных
циторедуктивных операций лишь на 3% [с 32 до 35% -8].
Еще в 80-е годы рядом авторов [3,4] показано,что больные с
распространенными и, в частности с асцитными формами рака
яичников, как правило, имеют значительное угнетение иммунного
статуса, симптомы анемии и интоксикации. Страдает перекисное
окисление липидов и антиоксидантная система крови [1]. В результате
лечение РЯ III-IY стадий с высокой интоксикацией остается во
многих аспектах не решенной проблемой. Требуется поиск не только
эффективной противоопухолевой терапии, но и препаратов,
направленных на снижение токсических проявлений [2,5].
Как правило, у больных раком яичников III-IY стадий высок
операционный риск и длительное время не удается начать
полихимиотерапию (ПХТ), повышается частота лейкопений. До
настоящего времени идут поиски подходов – с чего начинать лечение
рака яичников III-IY стадий: с циторедуктивной операции или
полихимиотерапии и каких препаратов. В связи с изложенным нами
использован реамберин, основой которого является янтарная кислота.
Превращение последнего в организме связано с «производством»
энергии, необходимой для обеспечения клеточной жизнедеятельности.
Мощность системы энергопродукции, замыкающейся на янтарной
кислоте, в сотни раз превосходит другие системы энергообразования.
Пополнение пула интермедиаторов цикла Кребса приводит к
увеличению скорости транспорта кислорода, снижению гипоксии и
эндотоксикоза [10].
Целью настоящей работы было изучение эффективности
применения отечественного препарата реамберин для снижения
интоксикации и побочных действий, которые являются основным
объектом, препятствующим эффективному применению специальной
терапии.
Материал и методы
Оценка состояния и степени выраженности интоксикации нами
проводилась у 171 больного по клиническим, функциональным и
биохимическим параметрам перед операцией, началом ПХТ и после ее
окончания через 3-4 недели в соответствии с рекомендациями ECOG-ВОЗ
по шкале токсичности [6].
Эффективность применения реамберина, оказывающего прямое
действие на окислительные процессы в цикле Кребса для снятия
интоксикации, тканевой гипоксии изучена у 89 больных асцитным раком
яичников III-IY стадий по классификации FIGO в возрасте от 42 до 79
лет после циторедуктивной операции и в процессе ПХТ (1группа). В
качестве контрольной группы взяты ретроспективные больные (82
пациентки) сравнительно аналогичные по возрасту и стадии
заболевания, оперированные в НОКОД и муниципальных больницах без
получения реамберина .
В таблице 1 представлены сравнительные данные состояния больных,
степени интоксикации и снижения показателей крови при поступлении в
НОКОД.
Таблица 1. Сравнительные данные степени интоксикации,
снижения показателей крови и статуса
больных раком яичников III-IY стадий до начала лечения
|
Группа б-х
|
Число б-х
|
Стадия
|
Статус больного
(ECOG -ВОЗ)
|
Степень интоксикации
|
Степень снижения показателей крови*
|
|
III
|
IY
|
II
|
III
|
IY
|
II
|
III
|
IY
|
0
|
I
|
II
|
III
|
|
1
|
89
|
73
|
16
|
17
|
48
|
24
|
16
|
47
|
26
|
9
|
35
|
26
|
19
|
|
2
|
82
|
65
|
17
|
15
|
42
|
25
|
13
|
44
|
25
|
7
|
32
|
25
|
18
|
|
Всего
|
171
|
138
|
33
|
32
|
90
|
49
|
29
|
91
|
51
|
16
|
67
|
51
|
37
|
* в большинстве случаев снижение показателей крови
констатировано по снижению уровня гемоглобина, реже тромбоцитов и
лейкоцитов
Даже оптимально выполненная циторедуктивная операция не спасает
от прогресса болезни, если не будет выполнена своевременно
адъювантная ПХТ.
В качестве стандарта 1-й линии ПХТ нами использованы препараты
платины, циклофосфамида и/или доксорубицина (жесткие, однодневные
схемы СР и САР), которые, наряду с высокой эффективностью, являются
нефро- и кардиотоксичные, что нельзя не учитывать. При наличии
анемии ниже 100 г/л подготовку к ПХТ во всех случаях начинали с
гемотрансфузий.
Применение реамберина впервые в онкологической практике при
однодневном (жестком) курсе ПХТ было использовано в Новгородском
областном клиническом диспансере [9]. Реамберин, основой которого
является янтарная кислота, в физиологических условиях
диссоциирована и носит название «сукцинат». Превращение последнего
в организме связано с «производством» энергии, необходимой для
обеспечения клеточной жизнедеятельности. Мощность системы
энергопродукции, замыкающейся на янтарной кислоте, в сотни раз
превосходит другие системы энергообразования. Пополнение пула
интермедиаторов цикла Кребса приводит к увеличению скорости
транспорта кислорода, снижению гипоксии и эндотоксикоза [10].
Реамберин вводили в виде 1,5% раствора перед операцией (1-2
дня), сразу после операции ежедневно (в/в, капельно не более 90
кап/мин в течение 5 –10 дней ) по 400 мл в сутки и в процессе
каждого курса ПХТ три дня подряд (до ПХТ, в день ПХТ и на следующий
день после ПХТ).
Послеоперационная ПХТ в обеих группах проводилась в комбинациях:
циклофосфан 750 мг/м2 + цисплатин 75 мг/м2 или цисплатин 50 мг/м2 +
циклофосфан 500 мг/м2 + доксорубицин 50 мг/м2 каждые три недели с
пре-и постгидратацией до 2-4 литров.
Таблица 2. Степень снижения гематологических показателей до
лечения
и в процессе ПХТ с применением реамберина и в контрольной
группе
| |
2 группа (контр. группа)
|
1 группа
(с реамберином)
|
|
До лечения
|
В процессе ПХТ
|
До лечения
|
В процессе ПХТ
|
|
Степень снижения гемоглобина
|
|
0 –> 115
|
70
|
49
|
76
|
79
|
|
1 –100 г/л-115
|
12
|
19
|
13
|
9
|
|
2- 80-100 г/л
|
-
|
10
|
|
1
|
|
3– 65-79 г/л
|
-
|
4
|
-
|
|
|
4- < 65 г/л
|
|
|
|
|
|
Cтепень снижения лейкоцитов
|
|
9
0- >4,0 х10
|
72
|
56
|
81
|
85
|
|
1- 3,0-3,9
|
10
|
18
|
8
|
3
|
|
2- 2,0-2,9
|
|
6
|
|
1
|
|
3- 1,0-1,9
|
|
2
|
|
|
|
4- <1,0
|
|
|
|
|
|
всего
|
82
|
82
|
89
|
89
|
В контрольной группе
число случаев анемий и лейкопений 1
степени
до начала ПХТ составило соответственно 12 (14,6±2,1%) и
10 (12,2±0,9%). В процессе курсов терапии показатели анемии и
лейкопении увеличились, включая 2-3 степень соответственно до 33
(40,2±3,6%) и 26 (31,7±3,2%). Тогда как во 1-й группе с применением
реамберина до лечения показатели составили соответственно 13
(14,6±2,1%) и 8 (8,9±0,5%), а в процессе курсов ПХТ
гематологические показатели практически не изменились (анемия 1-2
степени составила -11,2±1,1% и лейкопения - 4,4±1,6%. Разница числа
случаев и степени снижения гемоглобина и лейкоцитов в исследуемой
группе в сравнении с контрольной группой статистически достоверна
(p< 0,01).
Таблица 3. Степень нарушений функций сердца до лечения
и в процессе ПХТ с применением реамберина и в контрольной
группе
|
Степень нарушений
функций сердца
|
Контрольная группа
|
1 группа
|
|
До лечения
|
В процессе ПХТ
|
До лечения
|
В процессе ПХТ
|
|
0 – нарушений нет
|
20
|
7
|
18
|
23
|
|
1 – бессимптомное нарушение
|
19
|
20
|
21
|
21
|
|
2 – преходящая симптоматическая дисфункция, требующая лечения
|
26
|
32
|
27
|
23
|
|
3 – Коррегируемая дисфункция, нарушение ритма
|
17
|
23
|
23
|
22
|
|
Всего
|
82
|
82
|
89
|
89
|
Степень нарушения функций сердца 2 и 3 степени в
1группе, имеющаяся до леченияу 50 больных (56,1±3,7%),
позволили во всех случаях на фоне реамберина не только провести
полноценные курсы ПХТ, но и уменьшить частоту их нарушений до 45
(50,56±3,4%).
В контрольной группе число больных с нарушениями функций
сердца 2-3 степени в процессе химиотерапии, наоборот,
возросло с
52,4±3,4%
(43 больных)
до 67,1±4,1% (55 больной), требовались
коррегирующая терапия, увеличение сроков между курсами ПХТ или
уменьшение дозы препаратов. Разница статистически достоверна (p<
0,05) в сравнении с контрольной группой.
Одним из показателей оценки уровня нарушений мочевыделительной
системы является степень повышения креатинина. До начала лечения
повышение креатинина 1-й степени (таблица 4) констатировано
сравнительно одинаковым в 1-й (у 12 больных – 13,5%) и во второй
группах (у 11 больных – 13,4%).
Таблица 4. Степень повышения креатинина до лечения и в процессе
ПХТ
с применением реамберина и в контрольной группе
|
Степень повышения креатинина
|
2 группа (контр.группа)
|
1 группа
(с реамберином)
|
|
До лечения
|
В процессе ПХТ
|
До лечения
|
В процессе ПХТ
|
|
0 – нарушений нет (ВПН)*
|
71
|
48
|
77
|
88
|
|
1 – <1,5 Ч вН**
|
11
|
21
|
12
|
2
|
|
2 – 1,5-3,0 Ч вН
|
-
|
11
|
-
|
1
|
|
3 - 3,1-6,0 Ч вН
|
-
|
2
|
-
|
-
|
|
Всего
|
82
|
82
|
89
|
89
|
*ВПН-верняя граница нормы;
**Ч вН-число раз от верхней границы нормы.
В группе больных, получавших реамберин в качестве
предхимиотерапевтической подготовки и в процессе ПХТ лишь в 3-х
наблюдениях (3,37%) сохранилось повышение уровня креатинина, тогда
как в контрольной группе число больных с уровнем креатинина (1-3
степени) увеличилось у 34 больных (41,4%), что потребовала в 12
случаях (14,6%) приостановления химиотерапии, проведения
коррегирующей терапии. Разница между группами статистически
достоверна (p< 0,001).
При анализе других проявлений токсичности у больных, получающих
ПХТ на фоне реамберина, тошнота и рвота 1-2-й степени была
констатирована у 24 (26,9±2,2%) преимущественно отсроченная, в
контрольной группе 2 и 3 степень – у 45 (59,2±3,4%) больных, из них
у 28 острая (в течение 24 часов после начала химиотерапии),
несмотря на то, что за 30 мин до начала ХТ все больные получали
в/венно антимиметики (ондасетрон 8 мг или гранисетрон 1 мг).
Изучена динамика послеоперационных уровней сывороточного
СА-125 (высокомолекулярного гликопротеина, не
превышающиющего в норме 35 ед/мл) до начала ПХТ и в процессе
ее проведения, которая по мнению Н.С.Сергеевой с соавт.(2002)
является объективным предикторным фактором эффективности лечения
рака яичников. По данным большинства авторов уровень последнего
зависит не столько от объема опухолевых масс, сколько от вовлечения
в процесс мезотелия брюшины.
После 2 курса ПХТ по схеме СР (циклофосфан+платина)
или
САР
(циклофосфан + доксорубицин+платина)
уровень СА-125 выше
100 ед/мл
– в контрольной группе составил у большинства
68,2±4,2% (56 больных), в 1 группе – только у 21 больного
(23,5±1,9%, что более, чем в 2 раза ниже контрольной группы).
После 4 курса уровень маркера (менее 35 ед/мл) в 1 группе
достиг нормы – у 38,2±2,4% больных, тогда как во 2 группе он был
ниже нормы только у 13 больных (17,1±0,94%).
Таблица 5. Динамика послеоперационных уровней СА-125
в процессе ПХТ в обеих группах
|
Группы
|
Уровень Са 125 (ед/мл)
|
|
Более 1000
|
От 500 до 1000
|
От 300 до 500
|
От 100 до 300
|
От 35
до 100
|
<35
|
|
После операции
|
1
|
2
|
3
|
14
|
31
|
39
|
-
|
|
2
|
5
|
8
|
19
|
37
|
13
|
-
|
|
После 2 курса
|
1
|
|
-
|
2
|
19
|
57
|
11
|
|
2
|
|
6
|
12
|
38
|
23
|
3
|
|
После 4 курса
|
1
|
|
|
-
|
5
|
50
|
34
|
|
2
|
|
|
7
|
24
|
38
|
13
|
|
После 6 курса
|
1
|
|
|
|
|
11
|
78
|
|
2
|
|
|
|
16
|
39
|
27
|
Cтатистический анализ результатов исследования проводился в
системе SAS (Statistical Analisis System, SAS Institute Inc.,США) с
применением стандартных алгоритмов вариационной статистики, а также
программы STATISTICA 8.0. Анализ показал, что эффекты различий
снижения Са –125 после 2, 4 и 6 курса, значимые на уровне
р<0,05.
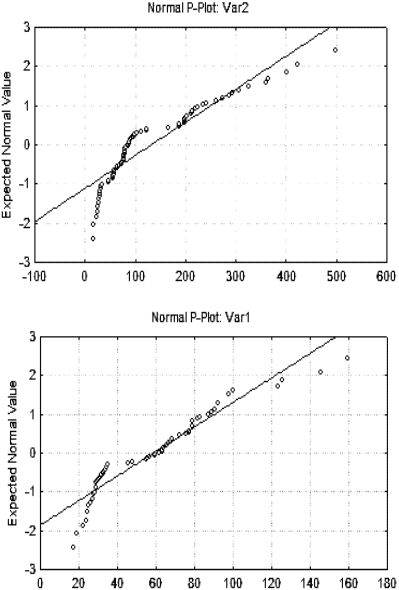
Рис 1. Сравнительные данные дисперсного анализа опухолевого
маркера Са-125
после 4 курса ПХТ в исследуемой группе с применением
реамберина (Var 1) и контрольной группе (Var2)
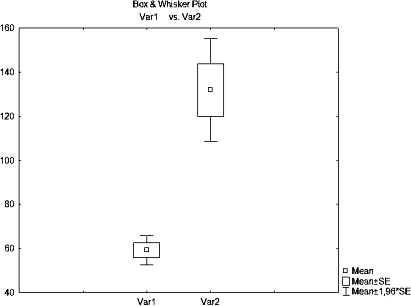
Рис 2. Уровни опухолевых маркеров Са-125 в 1 (var 1)
группе
в сравнении с контрольной группой (var 2)
Таким образом, исследования по применению 1,5% раствора
реамберина до циторедуктивной операции и сразу после операции, а
также в процессе последующей полихимиотерапии показали, что
реамберин является универсальным препаратом для снижения
интоксикации и протектором побочных действий специальной терапии
рака яичников без ослабления противоопухолевого эффекта.
Выводы
-
Использование препарата реамберин перед циторедуктивной
операцией и при однодневных(жестких) курсах полихимиотерапии
создает условия снижения опухолевой интоксикации и анемии.
-
Реамберин – универсальный протектор токсичности при ПХТ (с
использованием препаратов платины и доксорубицина). Применение
реамберина не сопровождается ослаблением противоопухолевого
эффекта.
-
Снижение опухолевого маркера СА-125 регистрируется в более
короткие сроки, чем в контрольной группе. Статастический анализ
показал, что эффекты различий снижения Са –125 после 2, 4 и 6
курса, значимые на уровне р<0,05.
Литература
-
Антонеева И.И. Перекисное окисление липидов и
ферментативное звено антиоксидантной системы крови при раке
яичников// Казан.мед.журнал.-2006.-№3.-с.158-166.
-
Винокуров В.Л. ,Юркова Л.Е., Буйнякова А.И.,
Максимов С.Я.и др. Современные аспекты химиотерапии
распространенного рака яичников. Материалы научно-практической
конференции «Новые подходы к скринингу, диагностике и лечению рака
яичников». Великий Новгород, 17-18 мая 2001, с.86-88.
-
Ласточкина В.И. . Иммунологическое обследование
больных новообразованиями яичников, Дис.на соиск. уч. степени
канд.мед.наук. М.1977;
-
Нечаева И.Д. Современные возможности диагностики и
лечения злокачественных опухолей яичников и перспективы развития
проблем. Вопр.онкологии,1984, 30,12,67-74.
-
Новикова Е.Г., Ронина Е.А.,Корнеева И.А.
Современные подходы в лечении злокачественных опухолей яичников.
Материалы научно-практической конференции «Новые подходы к
скринингу, диагностике и лечению рака яичников». Великий Новгород,
17-18 мая 2001, с. 112-115.
-
Руководство по химиотерапии опухолевых заболеваний.
Под ред. Н.И.Переводчиковой.2 издание. Практическая
медицина.Москва, 2005 с.661-691
-
Сергеева Н.С., Маршутина Н.В. Серологические
маркеры и их применение в клинической онкологии.// Избранные лекции
по клинической онкологии под ред.акад.РАМН В.И.Чиссова,
проф.С.Л.Дарьяловой. Москва, 2002, с.108-125.
-
Урманчеева А.Ф., ., Кутушева Г.Ф. Опухоли
яичника. В кн.: Лекции по фундаментальной и клинической онкологии
(под ред. В.М. Моисеенко, А.Ф.Урманчеевой, К.П.Хансон. Изд. Н-Л.
2004, с.319-359.
-
Черенков В.Г. , Чистякова Л.А. Пути снижения
побочных действий полихимиотерапии рака яичников III-IY стадий.-
Клиническая медицина (вопросы клиники, диагностики, профилактики и
лечения) В.Новгород-Алма-Ата, Межвузовск. Сборн., т.11, 2001,
164-167.
-
Яковлев А.Ю. Реамберин в практике инфузионной
терапии критических состояний, Санкт-Петербург, 2008, 32 с.

