Рис. 1. Динамика объема общей воды организма
у больных 1А, 2А, контрольной групп, M ± m
14.00.37 – анестезиология и реаниматология
Диссертация на соискание ученой степени кандидата медицинских наук
РОССИЙСКАЯ АКАДЕМИЯ МЕДИЦИНСКИХ НАУК
ГУ НАУЧНО-ИССЛЕДОВАТЕЛЬСКИЙ ИНСТИТУТ ОБЩЕЙ РЕАНИМАТОЛОГИИ
Назаров Борис Федорович
Научный руководитель: доктор медицинских наук, профессор, член-корреспондент РАМН, Мороз Виктор Васильевич
СОДЕРЖАНИЕ
|
Введение
|
Список сокращений:
Алан ин-глутамиламинотрансфераза - АЛТ
Артериальное давление диастолическое - АДд
Артериальное давление систолическое - АДс
Артериальное давление среднее - АДср
Аспартат-глутамиламинотрансфераза - АСТ
Биоимпедансная спектрометрия - БИС
Гамма-глутамиламинотрансфераза - ГГТ
Импеданс торса - ИмТ
Интерстициальная жидкость - ИЖ
Инфузионная терапия - ИнфТ
Кесарево сечение - КС
Кислотно-основное состояние - КОС
Минутный объем кровообращения - МОК
Общая вода организма - ОВО
Общее периферическое сопротивление - ОПС
Объем внеклеточной жидкости - ВКЖ
Объем клеточной жидкости - КЖ
Объем циркулирующей крови - ОЦК
Объемная компрессионная осциллометрия - ОКО
Полиорганная недостаточность - ПОН
Триглицериды - ТГ
Ударный объем сердца - УО
Холестерин - ХС
Холестерин высокой плотности - ХС ЛПВП
Холестерин липопротеиды низкой плотности - ХС ЛПНП
Холестерин липопротеиды очень низкой плотности - ХС ЛПОНП
Щелочная фосфатаза - ЩФ
АКТУАЛЬНОСТЬ. Несмотря на значительные достижения медицинской науки, в том числе и реаниматологии, сохраняется высокий процент осложнений и летальности у родильниц с преэклампсией в раннем послеродовом периоде. Так, по данным Кулакова В.И. и соавт., 1998, в мире ежегодно умирает 585000 женщин от причин, связанных с осложнениями беременности и родов, среди которых на долю преэклампсии приходится 20-30%. Больные с преэклампсией составляют основную группу риска по развитию различных осложнений в послеродовом периоде (Шалина Р.И., 1995).
В патогенезе преэклампсии ключевую роль играет генерализованный вазоспазм, повышение сосудистой проницаемости, задержка воды и натрия в организме с последующим развитием гипоксии, расстройством функции центральной нервной системы, почек, печени и других органов, глубоким нарушением обмена веществ. Сочетание гиповолемии и вазоспазма при тяжелой преэклампсии считается причиной синдрома гипоперфузии и тканевой гипоксии (Шифман Е.М., 2001). Отеки – один из триады симптомов этого осложнения беременности – являются лишь внешним проявлением нарушения распределения жидкости между внеклеточным и внутриклеточным секторами. При тяжелых формах преэклампсии дисгидрия и тканевая гипоксия сохраняются в послеродовом периоде (Абрамченко В.В., 2000). Эти изменения могут усугубляться, приводя к развитию полиорганной недостаточности.
Интерпретация общепринятых показателей диагностики преэклампсии и ее тяжести (артериальное и центральное венозное давление, величина периферических отеков, уровень белка крови и степень протеинурии и т.п.) у родильниц, зачастую, не дает представления о характере и выраженности патологического процесса, что затрудняет выбор лечебной тактики. В литературе имеются сообщения об исследовании водно-секторальных нарушений у беременных в различные гестационные периоды (Башмакова Н.В., Черданцева Г.А., Медвинский И.Д. и соавт., 2001; Шифман Е.М., 2000.). Однако нет данных о том, в течение какого времени после родоразрешения сохраняется водный дисбаланс, какую роль играют водно-секторальные нарушения в возникновении критических состояний у родильниц, требуется ли специфическая терапия для устранения дисгидрии. Классические методы исследования водных сред организма, например, разведение радиоизотопных индикаторов, бромида натрия и других веществ технически сложные и имеют высокий риск осложнений. Для неинвазивного определения водных секторов организма предложен метод биоимпедансной спектрометрии, об использовании которого у беременных и родильниц в литературе имеются единичные сообщения (Бахтина Т. П. , 2001; Plank L . D ., 1998 ) .
Следует отметить, что при проведении инфузионно-трансфузионной терапии особое значение приобретает применение объективных методов контроля водных секторов, гемодинамики, газообмена, метаболизма для оценки эффективности проводимого лечения родильниц с преэклампсией (Шифман Е.М., 2001).
Основными задачами инфузионной терапии в послеродовом периоде у
больных с тяжелой преэклампсией являются: коррекция объема и
реологических свойств крови, нормализация внеклеточного и
внутриклеточного секторов, улучшение микроциркуляции.
Патогенетически обосновано включение в комплексную терапию
растворов, нормализующих внутри- и внесосудистое распределение
жидкости и обладающих антигипоксическим действием. В настоящее
время в клинической практике для восстановления объема
циркулирующей крови и уменьшения интерстициальной гипергидратации
широкое распространение получили препараты на основе
гидроксиэтилкрахмала (Сидорова И.С., 2003, Шифман Е.М., 2001). Для
коррекции гипоксии и нормализации метаболических процессов в тканях
при ряде патологических состояний применяется раствор янтарной
кислоты – реамберин
(Оболенский С.В., 2003).
Таким образом, актуальным является исследование, направленное на выявление водно-секторального дисбаланса в послеродовом периоде у родильниц с преэклампсией и изучение влияния различных инфузионных растворов на гемодинамику, метаболический статус и распределение водных секторов у этой категории больных.
ЦЕЛЬ ИССЛЕДОВАНИЯ: Улучшить результаты лечения больных с преэклампсией путем оценки и коррекции водно-секторальных нарушений в послеродовом периоде.
Впервые получены данные о состоянии водных секторов в послеродовом периоде у родильниц с преэклампсией и при нормально протекающей беременности. Выя влена достоверная связь между степенью изменения водных секторов и тяжестью состояния в послеродовом периоде.
Показано, что дисгидрия в раннем послеродовом периоде у родильниц с преэклампсией проявляется в виде увеличения общей воды организма и объема интерстициальной жидкости.
Впервые получены данные о нормализации водно-секторальных нарушений, кислотно-основного состояния, биохимических показателей крови при комбинированной терапии гидроксиэтилированным крахмалом и реамберином в раннем послеродовом периоде у родильниц с преэклампсией.
Доказано, что инфузионная терапия гидроксиэтилкрахмалом и реамберином в раннем послеродовом периоде приводит к увеличению доставки и потребления кислорода, нормализации коэффициента экстракции кислорода, уменьшению проявлений гипоксии.
Состояние водных секторов определяет тяжесть состояния родильниц с преэклампсией.
Разработан алгоритм инфузионной терапии в послеродовом периоде родильниц с преэклампсией. Родильницам с тяжелой преэклампсией без нарушения кислотно-основного состояния в состав инфузионной терапии целесообразно включение гидроксиэтилированного крахмала. Родильницам с тяжелой преэклампсией и метаболическими нарушениями в 1-2 сутки после родоразрешения целесообразно в состав инфузионных сред включать реамберин и гидроксиэтилированный крахмал.
Метод биоимпедансной спектрометрии может применяться для определения вида дисгидрии и контроля эффективности проводимой терапии в раннем послеродовом периоде у родильниц с преэклампсией.
Внедрение в клиническую практику разработанного алгоритма терапии послеродового периода при тяжелой преэклампсии позволило уменьшить длительность лечения родильниц в отделении интенсивной терапии на 14%.
Работа выполнена в соответствии с планом НИР клинического отдела НИИ общей реаниматологии РАМН.
Результаты работы были доложены на международной конференции «Критические и терминальные состояния. Патофизиология и терапия», Москва, 2002; Конгрессе анестезиологов-реаниматологов Центрального федерального округа, Москва, 2003 г.; конференции «Критические технологии в реаниматологии», Москва, 2003; конференции «Реаниматология. Ее роль в современной медицине» Москва, 2004; на XI и XII Российских национальных конгрессах «Человек и лекарство», Москва, 2004, 2005; 4-ой и 6-ой сессиях МНОАР, Голицино, 2004, 2006; на открытом заседании Ученого Совета ГУ НИИ общей реаниматологии РАМН 21 апреля 2006 г .
Диссертация изложена на 115 страницах компьютерного текста, состоит из введения, 4-х глав (обзор литературы, характеристики клинических наблюдений и методов исследования, результатов исследования, обсуждения и заключения), выводов, практических рекомендаций. Работа иллюстрирована 11 таблицами, 23 рисунками. Указатель литературы включает 212 источников, из которых 72 отечественных и 140 зарубежных авторов.
Исследование динамики показателей водно-секторального баланса, гемодинамики, кислотно-основного состояния, биохимии крови в послеродовом периоде у родильниц с преэклампсией средней и тяжелой степени были выполнены в отделениях реанимации ГКБ им. С.П. Боткина и в родильном доме ГКБ № 70 в период с 2000 по 2004 гг. Обследовано 74 родильницы.
Исследование состоит из двух частей (А и Б).
В части А мы проводили сравнительную оценку водно-секторальных нарушений у здоровых родильниц и родильниц с преэклампсией в раннем послеродовом периоде.
В части Б - оценивали эффективность внутривенного применения гидроксиэтилированного крахмала и комбинированного использования растворов гидроксиэтилированного крахмала и реамберина в послеродовом периоде у родильниц с преэклампсией.
В части А обследовано 54 родильницы, которые были разделены на 3 группы (табл.1).
Таблица 1. Характеристика родильниц,
включенных в часть А исследования
|
Показатель |
Значения показателей |
||
|---|---|---|---|
|
1 группа (1А) |
2 группа (2А) |
Контрольная группа (К) (n=22) |
|
|
Возраст (годы) |
27,1±7,2 |
31,5±8,8 |
26,6 ± 4,6 |
|
Масса тела (кг) |
71,4 ±8,6 |
71,1 ±5,3 |
69,8 ± 7,2 |
|
Рост (см) |
164,8 ± 6,2 |
162,4 ± 6,7 |
165,7 ±7,1 |
|
Срок беременности при родоразрещении (нед) |
34-39 |
37-39 |
37-40 |
В 1-ю группу (группа 1А) вошли 20 родильниц с преэклампсией средней степени тяжести, состояние которых требовало наблюдения и лечения после родоразрешения в условиях палаты интенсивной терапии родильного дома.
2 группу (группа 2А) составили 12 больных с тяжелой преэклампсией, переведенные для лечения в отделение реанимации ГКБ им. С.П.Боткина. Степень тяжести по APACHE II больных 3 группы составила 22-28 баллов. Всем больным 3-й группы проводили контролируемую механическую вентиляцию легких с управляемым объемом (респираторы РВ-7200-АЕ), медикаментозную седацию диазепамом (0,02–0,25 мг/кг/час), дроперидолом (0,01-0.03 мг/кг/час), по показаниям использовались наркотические анальгетики (морфин 0,04-0,1 мг/кг/ч). Инфузионная терапия проводилась в соответствии с потребностями больных с динамическим контролем распределения водных секторов. 5 родильницам, в связи с развитием сепсиса, выраженными водно-секторальными нарушениями в комплекс терапии была включена гемофильтрация.
В контрольную группу включены 22 пациентки с нормально протекающей одноплодной беременностью, которым произведено кесарево сечение по различным причинам, не связанным с преэклампсией (дискоординация родовой деятельности, рубец на матке, поперечное положение плода).
В исследование части Б включены 42 родильницы. Все обследуемые в этой части исследования родильницы были разделены на 3 группы (табл.2).
1-я группа (1Б) включала 10 родильниц с тяжелой формой преэклампсии с нормальными показателями кислотно-основного состояния крови. Инфузионная терапия родильницам 1Б группы включала 6% раствор гидроксиэтилированного крахмала в объеме 5 мл/кг и физиологический раствор 5 мл/кг, которые вводили в первые сутки послеродового периода со скоростью 4-5 мл/мин.
Во 2-ю группу (2Б) вошли 10 родильниц с тяжелой преэклампсией и метаболическим ацидозом (в венозной крови ВE < -3,5; АВ < 22 ммоль/л). В состав инфузионной терапии больных этой группы входили растворы ГЭК и реамберина. Для инфузии использовали хета-гидроксиэтилированный крахмал с молекулярной массой 450 000 Д и реамберин, представляющий собой изотонический 1,5% раствор натрий-метилглюкаминовой соли янтарной кислоты со сбалансированным содержанием электролитов – натрия, калия, магния, хлора. Использовалась следующая методика введения: на первые сутки после родов последовательно внутривенно капельно вводили 6% раствор гидроксиэтилированного крахмала в дозе 5 мл/кг со скоростью 5 мл/мин и раствора реамберина в дозе 5 мл/кг - 4 мл/мин.
Таблица 2. Характеристика родильниц, включенных в часть «Б» исследования
|
Показатель |
Значения показателей |
||
|---|---|---|---|
|
1 группа (1Б) |
2 группа (2Б) |
Контрольная группа (К) (n=22) |
|
|
Возраст (годы) |
27,8±7,3 |
30,9±8,1 |
26,6 ± 4,6 |
|
Масса тела (кг) |
71,4±5,1 |
73,6±6,2 |
69,8 ± 7,2 |
|
Рост (см) |
163,1±5,4 |
162,2±7,6 |
165,7 ±7,1 |
|
Срок беременности при родоразрещении (нед) |
36-40 |
36-40 |
37-40 |
3-ю группу, контрольную, составили 22 родильницы с нормально протекающей одноплодной беременностью, которым было произведено кесарево сечение по различным показаниям, не связанным с преэклампсией (дискоординация родовой деятельности, рубец на матке, поперечное положение плода). Инфузионная терапия этим родильницам в первые сутки после кесарева сечения включала физиологический раствор в объеме 10 мл/кг, который вводился со скоростью 4 мл/мин.
Различий по степени тяжести преэклампсии, оцененной по шкале тяжести преэклампсии Американской ассоциации акушеров и гинекологов, между группами 1Б и 2Б не выявлено.
Протокол исследования. В части А исследование водно-секторальных и гемодинамических изменений проводили в три этапа: I этап – 1-е сутки после родоразрешения, исходное состояние; II этап – 3-и сутки послеродового периода; III этап – 5-е сутки после родоразрешения. Объем водных секторов определяли методом биоимпедансной спектрометрии. Оценивали общее содержание воды в организме, объем внеклеточной и интерстициальной жидкости, объем циркулирующей крови. Измерения на каждом этапе проводили троекратно, учитывая средний результат.
Биоимпедансная спектрометрия является методом неинвазивной оценки водных сред организма. Метод основан на измерениях импедансов (сопротивлений) тела на разных частотах. В используемом методе измерения выполняются на частотах 20 кГц (далее – низкой частоте – НЧ) и 500 кГц (далее – высокой частоте – ВЧ). На НЧ измеренный импеданс определяется в основном межклеточной средой, а на ВЧ – и межклеточной и внутриклеточной средами, так как мембраны клеток оказываются проницаемыми для тока на ВЧ. В результате измеренные импедансы на ВЧ оказываются меньше, чем импедансы тех же отведений на НЧ.
Используемый метод позволяет на основе измеренных значений импеданса регионов тела и других антропометрических параметров пациента (рост, вес, возраст, пол и т.д.) получить оценки состава тела, в числе которых: тощая (безжировая) масса тела, жировая масса, активная клеточная масса, общая вода организма, внеклеточная вода, внутриклеточная вода, объем циркулирующей крови, объем циркулирующей плазмы, интерстициальная жидкость.
В части Б исследование проходило также в три этапа, I этап – 1-е сутки после родоразрешения, до начала инфузионной терапии; II этап – 3-и сутки после родоразрешения; III этап – 5-е сутки послеродового периода. Кроме оценки водно-секторальных изменений биоимпедансным методом, осуществляли неинвазивный гемодинамический мониторинг методом объемной компрессионной осциллометрии с помощью прибора АПКО призводства ООО «Глобус». Оценивали АД, частоту сердечных сокращений, сердечный индекс, ударный индекс, общее периферическое сопротивление, расчетным методом определяли индекс доставки кислорода, индекс потребления кислорода и коэффициент экстракции кислорода.
Кислотно-основной статус определяли из проб артериальной и венозной крови газоанализатором ABL-500. Оценивали pH крови, буферную емкость (ВЕ), актуальный бикарбонат (АВ), сатурацию венозной крови (SvO2). Пробы крови забирались одновременно с измерением гемодинамики и определением водных секторов.
Оценку состояния системы кровообращения проводили методом объемной компрессионной осцилометрии. Измеряли следующие показатели кровообращения: артериальное давление (систолическое, диастолическое, среднее), частота сердечных сокращений, ударный и минутный объем кровообращения, сердечный индекс, ударный индекс, общее периферическое сопротивление.
Определение показателей биохимического состава плазмы крови осуществляли на автоматическом анализаторе Cobas Mira Plus . Кровь для исследования брали из вены на 1-е, 3, 5-е сутки после родов. В плазме крови определяли активность аланин-, аспартат-, гаммаглутаминотрансфераз (АЛТ, АСТ, ГГТ) и щелочной фосфатазы (ЩФ), а также концентрацию билирубина, общего белка, мочевины, креатинина и общего кальция. Для оценки состояния липидного обмена определяли концентрацию триглицеридов (ТГ), общего холестерина (ХС) и холестерина высокой, низкой и очень низкой плотности (ХС ЛПВП, ХС ЛПНП и ХС ЛПОНП).
Статистический анализ проводили с использованием пакета прикладных программ Statistica. Достоверность различий между группами оценивали по t –критерию Стьюдента при p < 0,05.
Часть А. Сравнительная оценка водно-секторальных нарушений у здоровых родильниц и родильниц с преэклампсией в раннем послеродовом периоде. При анализе водно-секторальных изменений в раннем послеродовом периоде выявлено, что при нормально протекающей беременности (контрольная группа) на первые сутки после родоразрешения общее количество воды в организме на 5,92± 1,34 л (р<0,05) больше, чем у небеременных (табл. 3).
Таблица 3. Изменения водных секторов в послеродовом периоде
при нормальной беременности, M ± m
|
Показатель |
Значения показателей |
|
|---|---|---|
|
Группа небеременных* |
Контрольная группа (n =22), 1 сутки |
|
|
ОВО, л |
42,72±4,31 |
48,64±6,93 |
|
ВКЖ, л |
11,83±1,29. |
14,80±4,71 |
|
КЖ, л |
31,06±5,76 |
32,46±8,94 |
|
ИЖ, л |
7,10±1,98 |
8,14±2,20. |
|
ОЦК, л |
4,57±0,72 |
5,15±0,96 |
|
ВКЖ/ОВО |
0,27 |
0,30 |
* - расчетные нормы, предлагаемые компьютерной программой аппарата АВС-01-Медасс
Для сравнения мы использовали нормы, разработанные производителями аппарата АВС-01-Медасс, которые были получены при обследовании небеременных женщин. Увеличено содержание внеклеточной жидкости на 2,97± 1,05 л (р<0,05), как за счет интерстициального компонента, так и ОЦК. Возрастает соотношение ВКЖ/ОВО, что отражает увеличение объема внеклеточной жидкости.

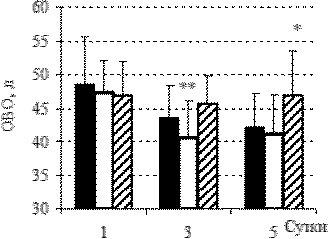
Рис. 1. Динамика объема общей воды организма
у больных 1А, 2А, контрольной групп, M ± m
Белые столбики – группа 1А,
полосатые столбики – группа 2А,
черные – контрольная группа.
* - достоверные различия с контрольной группой, р<0.05;
** - достоверные различия с первыми сутками в группе, p
<0,05.
У родильниц с преэклампсией на первые сутки после родоразрешения имеется увеличение общей воды организма по сравнению с небеременными в среднем на 5 л (табл.4, рис.1). Аналогичные изменения выявлены и в контрольной группе при нормально протекающей беременности. Однако у больных с преэклампсией увеличение ОВО происходит за счет внеклеточной жидкости, ее интерстициального компонента, тогда как в контрольной группе выявлено равномерное увеличение всех водных секторов. У больных с преэклампсией возрастает соотношение ВКЖ/ОВО до 0,35-0,37 по сравнению с контрольной группой (0,3) и расчетной нормой (0,27), что отражает увеличение объема внеклеточной жидкости. У родильниц в контрольной группе (здоровые родильницы) объем общей воды организма имеет тенденцию к снижению с 48,6 + 6,93 л в 1-е сутки после родов до 42,1 + 5,1 к 5 суткам.
Таблица 4. Динамика объема общей воды организма и объема
циркулирующей крови
у родильниц 1А, 2А и контрольной групп, M ± m
|
Сутки |
2А группа |
3А группа |
Контрольная группа (n=22) |
|||
|---|---|---|---|---|---|---|
|
ОВО, л |
ОВО, л |
ОЦК, л |
ОЦК, л |
ОВО, л |
ОЦК, л |
|
|
1 |
47,4±4,7 |
6,75±1,29 |
46,9±5,1 |
5,52±0,53 |
48,6±6,9 |
5,15±0,96 |
|
3 |
40,5±5,6** |
6,27±1,32 |
45,7±6,0 |
4,65±0,18 |
43,7±4,7 |
4,92±0,44 |
|
5 |
41,1±4,1 |
5,44±0,55 |
46,9±6,6* |
5,37±0,30 |
42,1±5,1 |
5,30±1,02 |
* - достоверные различия с контрольной группой, р<0,05
** - достоверные различия с первыми сутками в группе, p
<0,05
У больных 1А (преэклампсия средней тяжести) и 2А групп (тяжелая преэклампсия) ОВО в 1-е сутки не отличается от контрольной группы. К 3-им суткам в группе 1А отмечается достоверное снижение ОВО по отношению к 1-ым суткам, а в группе 2А у больных с тяжелой преэклампсией повышенное содержание ОВО остается в течение всего времени наблюдения и на 5 сутки достоверно выше (р<0,05), чем в контрольной группе – 46,9±6,6 против 42,1±5,1, что составляет 11,5%.
Таблица 5. Динамика внеклеточной и клеточной жидкости
у родильниц 1А, 2А и контрольной групп, M ± m
|
Сутки |
1А группа (n =20) |
2А группа (n =12) |
Контрольная группа (n =22) |
|||
|---|---|---|---|---|---|---|
|
ВКЖ, л |
КЖ, л |
ВКЖ, л |
ВКЖ, л |
КЖ, л |
ВКЖ, л |
|
|
1 |
17,5±4,3* |
28,7±6,3 |
15,3±1,5 |
32,1±4,5 |
14,8±4,7 |
32,5±8,94 |
|
3 |
14,1±3,4 |
25,9±5,6 |
14,8±1,2 |
28,9±5,0 |
12,3±1,5 |
30,5±3,49 |
|
5 |
12,9±1,3** |
27,8±4,4 |
15,6±1,3* |
30,9±4,1 |
11,7±2,4** |
29,8±5,5 |
* - достоверные различия с контрольной группой, р<0.05
** - достоверные различия с первыми сутками в группе,
р<0,05
Наибольшие различия между группами 1А, 2А и контрольной выявлены по объему внеклеточной и интерстициальной жидкости (табл. 5, рис.2). ВКЖ и ИЖ в первые сутки наблюдения у больных 1А группы выше, чем в контрольной группе на 2,7 л (18%) и 2,6 л (32%) соответственно. Но к 5 суткам объем ВКЖ снижается до 12,9±1,3 л, а ИЖ до 7,9±2,9 л , что не отличается от величин в контрольной группе.
У больных 2А группы с тяжелой преэклампсией объем внеклеточной жидкости оставался высоким в течение всего времени наблюдения и составил 15,6± 1,3 л против 11,7± 2.4 л в контрольной группе (увеличен на 33%). Такие же изменения наблюдались по объему интерстициальной жидкости: у больных с тяжелой преэклампсией на 5 сутки исследования объем ИЖ составил 9,8± 1,4 л , тогда как в контрольной группе – 6,9± 1,9 л (увеличен на 42%).
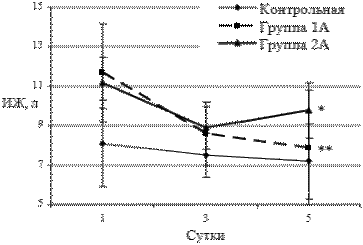
Рис. 2. Динамика объема
интерстициальной жидкости
у больных 1А, 2А, контрольной групп, M±m
* - достоверные различия с контрольной группой,
р<0.05
** - достоверные различия с первыми сутками в группе, p<0,05
У больных с преэклампсией средней тяжести имеется достоверное (р<0,05) увеличение внеклеточной и интерстициальной жидкости в 1-е сутки после родоразрешения по сравнению со здоровыми родильницами. К 5 суткам отмечали устойчивую тенденцию к нормализации объемов ВКЖ и ИЖ. У больных с тяжелой преэклампсией к 5 суткам после родоразрешения сохранялось достоверное (р<0,05) увеличение общей воды организма, внеклеточной и интерстициальной жидкости по сравнению с контрольной группой.
Часть Б. Оценка эффективности внутривенного применения гидроксиэтилированного крахмала и комбинированного использования растворов гидроксиэтилированного крахмала и реамберина в послеродовом периоде у родильниц с преэклампсией
Мы исследовали влияние комбинированного применения растворов гидроксиэтилированного крахмала (ГЭК) и реамберина на гемодинамику, метаболический статус и водно-секторальные нарушения у больных с тяжелой преэклампсией .
Для коррекции дисгидрии у родильниц с тяжелой преэклампсией мы применили раствор хета-гидроксиэтилированного крахмала. При выявлении у родильниц метаболического ацидоза, комплексная терапия включала комбинированное применение гидроксиэтилированного крахмала и препарата янтарной кислоты – реамберина.
У части больных с тяжелой преэклампсией наблюдался в послеродовом периоде метаболический ацидоз, уменьшение буферной емкости крови, низкую сатурацию венозной крови (табл.6). В связи с этим, все обследуемые больные с тяжелой преэклампсией были разделены на две группы: 1Б – с нормальными показателями кислотно-основного состояния и 2Б – с метаболическими нарушениями. Для коррекции метаболических нарушений в инфузионную терапию больных группы 2Б мы включили кроме гидроксиэтилкрахмала, раствор реамберина.
На фоне проводимой терапии ГЭК и реамберином у больных группы 2Б отмечается достоверное увеличение буферной емкости венозной крови к 3 суткам наблюдения. Сатурация венозной крови у больных группы 2Б в первые сутки была достоверно ниже, чем в контрольной.
Но в результате проводимой терапии к 5 суткам послеродового периода наблюдается достоверное увеличение SvO2 по сравнению с исходными данными (р<0,05). У родильниц 1Б и 3 (К) групп статистически значимых изменений КОС мы не определили.
При анализе показателей кислородного статуса выявлено (табл.7),
что у больных 1Б группы доставка кислорода исходно составила
504,9±31,6 мл/мин*м2 , что соответствует нижней границе
нормы. После инфузионной терапии ГЭК отмечается достоверное
повышение доставки кислорода по сравнению с первыми сутками
(рис.9). У больных 2Б группы в первые сутки послеродового периода
доставка кислорода снижена, не соответствует нормальным значениям и
меньше, чем у больных 1Б и 3 (К) групп. В процессе лечения после
инфузионной терапии растворами ГЭК и реамберина отмечается
достоверное увеличение доставки кислорода по сравнению с исходом. У
больных контрольной группы доставка кислорода в течение всего
времени наблюдения находилась в пределах нормальных значений (от
520,0±22,9 до 560,0±40,1 мл/мин*м 2 ).
Таблица 6. Динамика показателей кислотно-основного состояния
крови
у больных 1Б, 2Б и 3 (К) групп, M±m
|
Сутки |
pH a |
BE a |
pH v |
BE v |
АВ, v ммоль/л |
SvO 2 , % |
|---|---|---|---|---|---|---|
|
1Б (n=10) |
||||||
|
1 |
7,40±0,05 |
-2,28±1,44 |
7,37±0,07 |
-2,82±0,63 |
20,5±3,3 |
68,2±11,7 |
|
3 |
7,41±0,04 |
-1,32±0,27 |
7,38±0,04 |
-0,78±0,90 |
23,9±3,7 |
64,1±14,3 |
|
5 |
7,43±0,08 |
-0,57±0,95 |
7,37±0,03 |
-1,97±0,83 |
22,5±1,5 |
71,7±15,2 |
|
2Б (n=10) |
||||||
|
1 |
7,41±0,03 |
-3,85±1,46 |
7,33±0,07 |
-5,57±1,19 |
18,32±3,5 |
54,3±12,6** |
|
3 |
7,39±0,04 |
-1,49±0,93 |
7,35±0,05 |
-1,87±1,27* |
23,12±2,7 |
66,8±17,1 |
|
5 |
7,42±0,03 |
-0,98±0,91 |
7,35±0,03 |
-2,55±0,59 |
22,28±2,5 |
71,6±11,4* |
|
Контрольная (n=22) |
||||||
|
1 |
7,42±0,02 |
0,3±0,34 |
7,38±0,03 |
-1,2±0,91 |
24,6±2,1 |
78,1±4,6 |
|
3 |
7,40±0,03 |
1,0±0,41 |
7,37±0,02 |
-0,9±0,02 |
26,1±3,4 |
77,4±5,2 |
|
5 |
7,41±0,03 |
1,9±0,54 |
7,40±0,04 |
1,1±0,88 |
25,4±2,7 |
74,1±6,0 |
* - достоверные различия с первыми сутками в группе,
p<0,05.
** - достоверные различия с контрольной группой, р<0,05.
Величина потребления кислорода у больных с тяжелой преэклампсией без нарушений КОС была 150-180 мл/мин*м2, что соответствует нормальным показателям (табл.7). Однако в группе больных с метаболическими нарушениями в первые сутки наблюдения потребление кислорода и коэффициент экстракции кислорода были достоверно ( p <0,05) выше, чем в контрольной (иПО 2 217,0±23,6 против 137,7±18,2; КЭО 2 44,4±8,7 против 26,0±3,7) (рис.3).
Таблица 7. Показатели гемодинамики и баланса кислорода
у больных 1Б, 2Б и контрольной групп, M±m
|
Сутки |
АД ср, мм рт.ст. |
СИ, мл/мин*м 2 |
ОПСС, дин*с*см -5 |
иДО 2, мл/мин*м2 |
иПО 2, мл/мин*м2 |
КЭО 2 , % |
|---|---|---|---|---|---|---|
|
1Б (n=10) |
||||||
|
1 |
80,0±11,1 |
3,46±1,20 |
1233±264 |
504,9±31,6 |
151,0±19,1 |
29,9±4,1 |
|
3 |
85,8±11,2 |
3,87±1,33 |
1209±187 |
533,5±49,4 |
183,0±17,6 |
34,3±6,0 |
|
5 |
78,3±13,3 |
3,60±1,06 |
1141±206 |
570,0±56,3* |
166,5±20,4 |
29,0±5,1 |
|
2Б (n=10) |
||||||
|
1 |
98,7±10,3 |
3,49±0,72 |
1333±327 |
488,8±57,3 |
217,0±23,6** |
44,4±8,7** |
|
3 |
88,6±12,8 |
3,99±1,01 |
1177±213 |
618,4±33,5** |
235,0±16,8** |
38,0±4,6 |
|
5 |
97,2±6,4 |
4,09±1,13 |
1283±170 |
654,5±50,9* |
242,8±18,2** |
37,1±5,5* |
|
3 Контрольная (n=22) |
||||||
|
1 |
82,4±8,4 |
3,32±0,78 |
1155±161 |
520,0±22,9 |
137,7±18,2 |
26,0±3,7 |
|
3 |
91,6±7,3 |
3,09±0,42 |
1187±182 |
540,0±38,4 |
144,5±20,3 |
28,7±4,3 |
|
5 |
89,1±10,2 |
3,18±0,55 |
1196±123 |
560,0±40,1 |
161,8±13,8 |
24,5±3,9 |
* - достоверные различия с первыми сутками в группе,
p<0,05
** - достоверные различия с контрольной группой, р<0,05
После инфузионной терапии ГЭК и реамберином потребление кислорода у больных 2Б группы еще больше возростало, но уменьшился коэффициент экстракции кислорода (табл. 7, рис.4), что является благоприятным признаком и отражает положительную динамику. Коэффициент экстракции кислорода у больных 1Б и контрольной групп был в пределах нормальных значений. У родильниц 2Б группы КЭО 2 в 1-е сутки достоверно выше, чем в контрольной группе. Но на фоне проводимой терапии, при повышении доставки и потребления кислорода, КЭО 2 снижался к 5 суткам. Величина сердечного индекса у больных всех трех групп колебалась в пределах нормальных значений, достоверных отличий между группами выявлено не было.
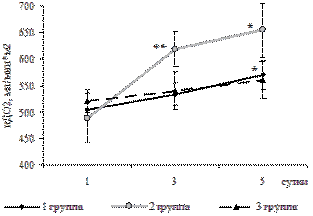
Рис. 3. Динамика индекса доставки кислорода
у родильниц 1Б, 2Б и контрольной групп, M ± m
* - достоверные различия с первыми сутками в
группе, p<0,05.
** - достоверные различия с контрольной группой, р<0,05.
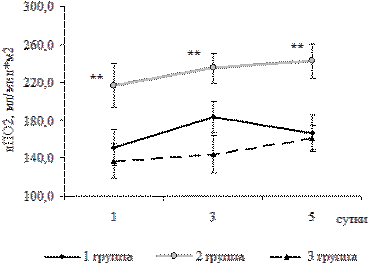
Рис. 4. Динамика индекса потребления кислорода
у родильниц 1Б, 2Б и контрольной групп, M ± m
* - достоверные различия с первыми сутками в
группе, p<0,05.
** - достоверные различия с контрольной группой, р<0,05
Общее периферическое сосудистое сопротивление у больных с преэклампсией было выше, чем в контрольной группе, но эти изменения не имели достоверный характер.
Выявлено, что у больных 1Б и 2Б групп доставка кислорода после инфузии ГЭК и реамберина увеличивается. Однако значение потребления кислорода изменяется только в группе больных с нарушениями КОС: в течение всего времени наблюдения оно достоверно выше, чем в контрольной группе и имеет тенденцию к увеличению.
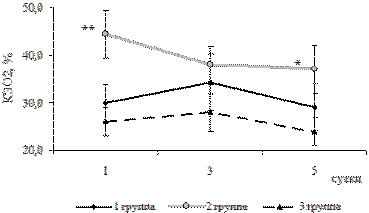
Рис. 5. Динамика коэффициента экстракции кислорода
у родильниц 1Б, 2Б и 3(К) групп, M ± m
* - достоверные различия с первыми сутками в
группе, p<0,05.
** - достоверные различия с контрольной группой, р<0,05.
У больных 1Б и 2Б групп исходно отмечается значительная гипергидратация – объем ОВО увеличен более чем на 15% по сравнению с контрольной группой в основном за счет интерстициальной жидкости (табл.7). Увеличение ИЖ составляет 20% для больных 4.1 группы и 25% для 4.2. У больных 1Б и 2Б групп отмечена относительная гиповолемия – по сравнению с контрольной группой ОЦК снижен на 10-15%. После инфузии ГЭК в 1Б группе наблюдается достоверное снижение объема ИЖ, и к 5 суткам он сопоставим с данными в контрольной группе. ОЦК у больных 1Б группы после инфузии ГЭК имеет тенденцию к увеличению, хотя ограничения методики не позволяют выявить достоверных закономерностей. В 2Б группе после комбинированного применения ГЭК и реамберина также отмечается положительная тенденция – ИЖ и ОВО достоверно уменьшаются к 5 суткам, величина ОЦК соответствует показателю в контрольной группе.
Таблица 9. Динамика показателей водно-секторальных изменений
у больных 1Б, 2Б и контрольной групп, M±m
|
Сутки |
ОВО 1 |
ВКЖ 1 |
КЖ 1 |
ИЖ 1 |
ОЦК 1 |
Импеданс торса, Ом |
|---|---|---|---|---|---|---|
|
1Б (n=10) |
||||||
|
1 |
119,4±16,6 |
128,2±14,4 |
107,5±12,3 |
129,4±17,8 |
104,3±9,7 |
2,71±0,38 |
|
3 |
111,2±14,1 |
116,2±15,8 |
99,5±13,2 |
121,4±15,5 |
103,6±13,9 |
2,90±0,35 |
|
5 |
99,6±7,5* |
100,2±8,8* |
97,7±7,4 |
106,4±9,9* |
107,5±7,4 |
3,12±0,42 |
|
2Б (n=10) |
||||||
|
1 |
123,8±15,2 |
132,7±9,2 |
118,9±15,2 |
134,5±16,7 |
109,4±14,5 |
2,92±0,38 |
|
3 |
115,7±9,4 |
123,3±13,3 |
113,7±8,5 |
124,7±17,0 |
107,7±15,7 |
3,10±0,57 |
|
5 |
106,7±9,7* |
105,6±11,4* |
101,6±10,3 |
108,1±11,8* |
104,2±16,2 |
3,19±0,36 |
|
3 Контрольная (n=22) |
||||||
|
1 |
115,5±10,2 |
112,7±13,4 |
98,3±9,6 |
109,6±12,1 |
118,9±10,1 |
3,28±0,41 |
|
3 |
98,8±12,6 |
102,4±12,8 |
91,2±8,1 |
100,8±9,1 |
113,6±9,5 |
3,23±0,34 |
|
5 |
103,5±9,9 |
101,3±11,4 |
96,7±7,7 |
97,3±8,4 |
108,5±13,3 |
3,45±0,29 |
* - достоверные различия с первыми сутками в группе,
p<0,05.
1 - в % по отношению к расчетной норме, предлагаемой
компьютерной программой аппарата АВС-01-Медасс.
У родильниц с тяжелой преклампсией без нарушений КОС инфузия гидроксиэтилированного крахмала в 1-2-е сутки после родоразрешения уменьшает содержание общей воды организма, внеклеточной и интерстициальной жидкости, увеличивает доставку кислорода. У родильниц с тяжелой преэклампсией и метаболическим ацидозом комбинированная инфузионная терапия гидроксиэтилированным крахмалом и реамберином в 1-2-е сутки послеродового периода приводит к увеличению доставки и потребления кислорода, уменьшению интерстициальной гипергидратации и нормализации кислотно-основного состояния.
При нормально протекающей беременности на первые сутки после родоразрешения общее количество воды в организме по нашим данным на 5,92± 1,34 л больше, чем у небеременных. Увеличено содержание внеклеточной жидкости, как за счет интерстициального компонента, так и ОЦК. Полученные данные согласуются с имеющимися в литературе сообщениями, где показано, что увеличение ОВО в поздних сроках беременности и раннем послеродовом периоде составляет около 6 л (Scardo J.A ., 2000). По данным Hytten и Томас, за время беременности ОВО увеличивается на 7,76 л. Хотя общее содержание воды в организме увеличивается на 7-9 л (Абрамченко В. В., 2000) , при нормально протекающей беременности отеков не возникает. Это происходит за счет дилятации артериол, увеличения емкости сосудистого русла. Такие изменения баланса воды в организме можно расценить как физиологические.
В ходе нашего исследования выявлено, что у родильниц с тяжелой преэклампсией в течение всего времени наблюдения сохраняется повышенное содержание общей воды организма; показатели внеклеточной и интерстициальной жидкости оставались достоверно выше по сравнению с контрольной группой.
Увеличение интерстициальной жидкости при тяжелой преэклампсии описано как феномен «третьего водного сектора». «Третий водный сектор» формируется за счет секвестрации жидкости на периферии, а также увеличения жидкости в плаценте, околоплодных водах, в самом плоде (Зильбер А.П., Шифман Е.М., 1997) . При преэклампсии, эклампсии происходит нарушение механизмов адаптации за счет гемодинамических, метаболических, коллоидно-осмотических расстройств. Гиповолемия, характерная для тяжелой формы преэкалмпсии, является одним из мощных стимулов избыточной секреции АДГ и увеличения ретенции жидкости.(Р ед. В.И. Кулакова. – 2000).
У больных с преэклампсией мы наблюдали незначительное увеличение ВКЖ. Известна и безотечная форма (у 32% больных) эклампсии, которая является наиболее опасной в прогностическом плане. Перинатальная смертность у таких женщин значительно выше, чем у беременных с преэклампсией, протекающего на фоне выраженного отечного синдрома (Серов В.Н., 2002; Lopot F , 2001) .
При преэклампсии интерстициальная гипергидратация развивается вследствие резкого увеличения проницаемости эндотелия для белка. В условиях эндотелиального повреждения жидкость не в состоянии длительно удерживаться в сосудистом русле (Мороз Б.Б., 2001). Вследствие интерстициального отека легких происходит более раннее экспираторное закрытие дыхательных путей, гиповентиляция обширных зон легких, увеличение шунтирования крови, усугубление гипоксии, что ведет к развитию ОПЛ.
Выявленный в ходе нашего исследования эффект нормализации КОС у больных с тяжелой преэклампсией при использовании реамберина согласуется с литературными данными. Ряд авторов (Исаков В.А., с соавт., 2001) в своих исследованиях показали эффективность реамберина у больных в критических состояниях за счет антигипоксического, антиоксидантного действия препарата. Основной фармакологический эффект реамберина обусловлен способностью усиливать компенсаторную активность аэробного гликолиза, снижать степень угнетения окислительных процессов в цикле Кребса в условиях гипоксии с увеличением содержания АТФ и креатинфосфата. Реамберин активирует антиоксидантную систему ферментов и тормозит процессы перекисного окисления липидов в ишемизированных органах (Оболенский С.В., 2003). Таким образом, нормализацию КОС у больных 2Б группы можно объяснить не только за счет увеличения доставки кислорода на фоне инфузионной терапии, но и непосредственным влиянием реамберина на метаболические процессы в тканях.
По результатам нашего исследования, у родильниц 2Б группы исходно выявлены низкая доставка кислорода, высокое потребление, высокий коэффициент экстракции кислорода, низкая сатурация венозной крови. В результате лечения мы наблюдаем увеличение доставки кислорода с параллельным увеличением потребления, что может свидетельствовать о патологической зависимости потребления кислорода от доставки и формировании кислородной задолженности в тканях ( Shoemaker W . C ., et al .- 1992). В дальнейшем в ходе терапии доставка и потребление кислорода достигают оптимального для данной группы больных уровня, коэффициент экстракции кислорода снижается, уменьшается тканевая гипоксия. Как следствие этого мы наблюдаем нормализацию рН крови и буферной емкости, увеличение сатурация венозной крови.
Комбинированное применение ГЭК и реамберина позволило сочетать положительные эффекты обоих препаратов: увеличить доставку кислорода путем нормализации внутрисосудистого объема, уменьшения интерстициальной гипергидратации раствором ГЭК и улучшить оксигенацию тканей за счет антигипоксического и антиоксидантного действия реамберина.
Проведенное комплексное исследование позволило выявить ведущие звенья водно-секторальных нарушений в послеродовом периоде у родильниц с преэклампсией различной степени тяжести. На этой основе были разработаны алгоритмы инфузионной терапии в зависимости от степени тяжести преэклампсии, вида дисгидрии и кислотно-основного статуса.
Одним из наиболее важных компонентов терапии является скорейшая нормализация распределения жидкости и коррекция метаболических нарушений. Ликвидация водно-секторальных и метаболических нарушений в раннем послеродовом периоде у родильниц с преэклампсией не решает всех проблем у больных в критических состояниях, но является обязательным условием успешной терапии.
Применение на практике разработанных алгоритмов инфузионной терапии с учетом показателей баланса водных секторов и кислотно-основного статуса способствовало улучшению результатов лечения, снижению сроков пребывания в послеродовом периоде родильниц с преклампсией в отделении интенсивной терапии на 14% .